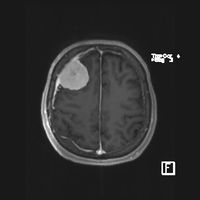
Meningeom
Indholdsfortegnelse
Indledning
Meningeomer er langsomt voksende tumor som typisk er relateret til hjernehinderne omkring hjernen eller rygmarven. De menes at udgå fra den miderste hjernehinde araknoidea(villi arachnoidale-cellerne). 90% af de intrakranielle meningeomer er lokaliseret supratentorielt. Under 2% findes ekstraduralt. Det kan være i orbita, parafaryngealt, cavum nasi, næsens bihuler eller cavum oris. En anden sjælden lokalisationer at i hjernens ventrikelssystem.
Meningeomer udgør ca. 20% af primære intrakranielle tumorer, og de er dobbelt så hyppige hos kvinder. Incidensen er stigende med alderen, under 1% findes hos børn. De kan vokse som en solitær tumor, der skubber hjernen foran sig eller en plaque med en fladeformet udbredning langs dura og kranium. De kan vokse infiltrativt i theca eller basis cranii, og kan give anledning til en lokal fortykkelse af kraniet uden indvækst i dette (hyperostosis). De kan være omgivet af et betydeligt ødem. Multiple meningeomer ses hos ca. 15%.
Epidemiologi
Prævalensen er ca. 2-2,5%. Der er en markant overhyppighed hos kvinder ca. en faktor 1,8 mere end hos mænd. Forskellen mellem hyppigheden hos mænd og kvinder er aldersafhængig og størst i aldresgruppe 35-44-årige hvor den er 3,15. I modsætning til den generelle overhyppighed af meningeomer hos kvinder er der en mindre overhyppighed af atypiske og maligne meningeomer hos mænd. En meget stor andel af meningeomerne er symptomatiske, således blev der i 2016 "kun" registreret 759 nye tilfælde i Danmark, sv.t. en incidens på ca. 1,2/100.000. Incidensen har været støt stigende igennem en årrække og dette forventes at forsætte i takt med at der gennemføres langt flere skanninger, særligt MR-skanninger af hjernen. En prævalens på 2,5% sv.t. at knap 150.000 danskere har meningeomer.
Ætiologi
- Der er en overhyppighed af meningeomer hos personer med Neurofibromatosis type 2 (NF2) som skyldes skyldes mutationer i NF2 genet, et tumorsuppressorgen lokaliseret på kromosom 22 (22q12.2)
- Ioniserende stråling er en kendt men sjælden årsag i Danmark. Meningeomer induceret af stråling er oftere end normalt maligne.
- Køn, det er uvist hvorfor kvinder har en større hyppighed end mænd, der er ikke fundet en sikker hormonel forklaring
- Mobiltelefoni har været rejst som risikofaktor, der er på trods af mange studier intet belæg for dette
Histologi
Meningeomer inddeles i de benigne (85%), atypiske (10%) og anaplastiske (5%). Benigne meningeomer er langsomt voksende tumorer og ofte ses meget store meningeomer, som har givet anledning til forbavsende få symptomer.
Meningeomgradering – diagnostiske kriterier WHO 2016
WHO grad 1 typisk meningeom uden tegn på atypi (WHO grad 2) eller anaplasi (WHO grad 3).
WHO grad 2 Atypisk meningeom defineret ved
- Øget mitotisk index: mere end 4, men mindre end 20 mitoser på 10 High Power (x40) Field (HPF – defineret som 0.16mm2 ) eller
- Hjerneinvasion bedømt ud fra histologien og/eller 3 af følgende tegn til atypi: øget cellularitet, små celler med høj kerne/cytoplasma ratio, prominerende nucleoli, tab af lobulær arkitektur (solid-patternless), * foci af ”spontan” nekrose, der ikke kan forklares ved præoperativ Chordoid meningeom
- Clear celle meningeom (intrakranielt)
- tumor-embolisering
OBS: Hjerneinvasion Invasion i hjernen i form af irregulære, tungelignende protusioner af tumorceller ind i parenkymet uden mellemliggende leptomeninges medførende reaktiv astrocytose. Tilstedeværelsen af hjerneinvasion peger på større recidiv-hyppighed og er tegn på atypi / anaplasi.
WHO grad III Anaplastisk meningeom – defineret ved
- Øget mitotisk index: 20 eller flere mitoser per 10HPF – og/eller
- Tydelige tegn på malignitet i forhold til kriterier som under atypi beskrevet
Papillært meningeom
Rhabdoidt meningeom
Symptomer
Symptomer ved meningeomer er som ved andre hjernetumorer, de kan inddeles i 3 kategorier:
- Lokal dysfunktion: Disse symptomer skyldes at tumor komprimerer hjernen samt det nogle gange meget betydelige ødem omkring tumor. Fokale symptomer er helt afhængige af tumors lokalisation, fx ændret psykisk adfærd ved store olfactorius meningeomer. Et sjældnere men differentialdiagnostisk vigtigt symptom er supranukleære paraparesis inferior ved falx meningeom som komprimerer begge mesiale frontallapper sv.t. benets motoriske cortex, dette kan forveksles med eksempelvis cervikal stenose.
- Irritative symptomer: Lang det hyppigste irritative symptom ved meningeomer er epilepsi, for praktiske formål kun ses ved de supratentorielle meningeomer. Smerte ses nogle gange unden større masseeffekt, dette skyldes formodentligt den lokale irritation af dura.
- Tryksymptomer: Hovedpine, kvalme og opkastninger.
Billeddiagnostik
Meningeomer er ofte næsten isodense med hjernen på henholdsvis CT og T1-vægtede MR billeder. Efter intravenøs kontrast ses typisk en homogen kontrast opladning. På MR-skanningen ses efter kontrast en "dural tail" i ca. 60%, som er en kontrastopladning i dura rundt om meningeomets tilhæftning. 10-15 % af meningeomer har et atypisk udseende på MR såsom heterogen kontrastopladning, cyster, ringopladning, blødning og fedtlignende indhold, hvorved de kan ligne metastaser eller maligne gliomer. Ved meningeomer nær hjernens venøse sinus er det relevant at supplere med en MR-angio, for at se om sinus er lukket. Et stigende antal meningeomer diagnosticeres ”tilfældigt”, hvorved vi forstår meningeomer, som findes ved en skanning, men ikke forklarer patientens symptomer.
PET-skanning 68Ga –DOTATOC og DOTATATE PET skanning er meget sensitivt for meningeom væv, og kan identificere ca. 10 % flere, men ofte små, meningeomer end konventionel MR. PET anvendes primært hvis der er tvivl om antal eller udbredning af meningeomer, samt til at skelne mellem aktivt tumor væv og reaktive forandringer efter tidligere behandling.
Behandling
Kirurgi
Den primære behandlingsform er kirurgi, men det skal huskes at mange meningeomer aldrig giver symptomer, hvorfor det ikke er indikeret kirurgisk af fjerne alle påviste meningeomer. Den samlede gevinst og risiko for patienten skal nøje afvejes.
Indikation for kirurgi
- Masseeffekt (kompression af gyri med signal på FLAIR) herunder ødem.
- Symptomer/epileptisk anfald
- Påvist vækst
- Patientens ønske
- Risiko for forværret prognose ved at udsætte kirurgi (specielt for skull base meningeom)
Relative kontraindikationer
- Høj alder
- Komorbiditet
- Vanskelig lokalisation
- Kort forventet restlevetid
Ved kirurgisk fjernelse anbefales det et stykke af den omkringliggende dura også fjernes, sv.t. dural tail på MR, som i nogle studier er vist at indholde meningeom tumorceller. Selve den kirurgiske teknik varierer helt efter lokalisation og kan varierer fra at være en relativ simple procedure ved mindre konveksitets meningeomer uden ind vækst i cortex til større skull base meningeomer i svært tilgængelige lokalisation som kan omskede kar og nervestrukturer.
Graderinger af kirurgisk fjernelse
Der anvendes aktuelt primær 2 forskellige graderingssystemer af kirurgi, den ældre Simpson gradering fra 1957 og den nyere EORTC/RTOG baseret på MR-skanninger efter operationen. I nyeste guideline fra EANO anbefales som minimum dette suppleret med postoperativ MR enten efter 48 timer eller 3 måneder.
Simpson gradering med EORTC/RTOG i parentes (GTR = komplet fjernelse; STR = partiel fjernelse)
- Grad 1 Makroskopisk komplet fjernelse af tumor, inklusiv fjernelse af omkringliggende dura, abnorm knogle og venøs sinus hvis der er indvækst (GTR)
- Grad 2 Makroskopisk komplet fjernelse af tumor med koagulation af omkringliggende dura (GTR)
- Grad 3 Makroskopisk fjernelse af den intradurale tumor komponent uden behandling (fjernelse / koagulation) af ekstradurale dele af tumor eller omkringliggende dura (GTR)
- Grad 4 Partiel fjernelse af tumor (STR)
- Grad 5 Dekompression af tumor / biopsi
Der er i flere studier påvist sammenhæng med Simpson grad og risiko for genvækst af tumor.
Komplikationer til kirurgi
Mortalitet (døds) risikoen afhænger af mange forhold, herunder pateintens alder, tumor lokalisation, andre samtidige sygdomme samt naturligvis kirurgens kvalifikationer. I Nogle studier er der fundet over 5% mortalitet hos patienter over 65 år.
Morbiditetsfrekvens (nye symptomer efter operation) varierer i forhold til, hvad der opfattes som morbiditet. Et hollandsk studie (van der Vossen et al) fandt, at 40% har kognitive og/eller emotionelle problemer postoperativt, herunder depression hvor tidligere nævnte meta-analyse hos plus 65-årige har en komplikationsrisiko på 20 %. Postoperativ epilepsi kan ligeledes opfattes som morbiditet og har alene en risiko på 12 %.
Strålebehandling
Strålebehandling anbefales som rutine postoperativ behandling til grad 3 meningeomer, og kan anvendes ved grad 1 og 2 meningeomer hvor der ikke kan opnår kirurgisk kontrol. Hvor det er muligt i forhold til risici foretrækkes stereotaktisk radiokirurgi (SRK) som er en velafgrænset engangs strålebehandling med stråle dosis, når dette ikke muligt benyttes konventionel fraktioneret strålebehandling.
Fraktioneret strålebehandling af meningeomer medfører stort set aldrig totalt tumorsvind. I stedet opereres med begrebet ”tumorkontrol”, hvorved forstås, at der ved efterfølgende neuroradiologiske undersøgelser ikke påvises vækst af tumor. Tumorkontrol indbefatter således både partiel regression og stationære forhold. Graden af tumor kontrol er fundet meget varierende i forskellige studier og afhænger meget af opfølgningstiden som i mange studier er for kort til at være relevante. Det samme problem gælder komplikationer til strålebehandling som kræver langtidsopfølgning.
Andet
Behandlingsresponsen ved systemisk behandling (kemoterapi) af recidiverende meningeomer, når der ikke længere kan tilbydes operation eller strålebehandling, er dårlig. Der har været afprøvet flere medicinske behandlingsprincipper uden effekt.
Behandlings algortime
Danske anbefalinger fra 2018
Meningeom grad 1
- Observation: Incidentielle små meningeomer uden masseefekt og symptomer observeres initielt. Første skanning 3-6 måneder af differential-diagnostiske årsager, derefter 1,3,5,7 og 10 år efter første observation. Kan afkortes ved høj alder.
- Kirurgi: der stræbes efter GTR defineret som Simpsom grad 1, 2 og 3.
- Strålebehandling: ved små tumorer, personer over 65 år eller svært tilgængeligt tumorer, kan der behandles med stereotaktisk strålebehandling (5 års PFS (progression free survival) er 86 – 100%). Hvis større kan fraktioneret RT gives (54 Gy på 1,8 til 2,0 pr fraktion), 5 års PFS er 75 – 92%.
- Kombination: af kirurgi og SRT giver 5 års PFS som ved GTR.
- Opfølgning: GTR konfirmeres ved 3 måneders MR med kontrast. Herefter 1, 3, 5, 7 og 10 år efter operation. Samme opfølgning anbefales ved kombinationsbehandling.
- Ved kendt subtotal resektion er recidiv-risiko på 10 år mellem 55 og 100 %.
- For GTR er recidiv-risiko på 10 år mellem 20 og 39 %.
Meningeom grad 2
- Observation: ved tidligere strålebehandling er risikoen for, at meningeomer grad II højere.
- Behandling: Kirurgi: der stræbes efter GTR defineret som Simpsom grad 1, 2 og 3.
- Strålebehandling: der foreligger IKKE valide studier til at anbefale up-front RT ved GTR (Prospektive randomiserede studier på vej). Ved inkomplet fjernelse (STR) bør RT overvejes, men der foreligger alene data til at anbefale RT ved sikker progression (med eller uden kirurgi først). Standard fraktioneret RT bør vælges fremfor stereotaktisk strålebehandling. Obs: langtidsrisiko for strålefølger er 53 % over 12 år. Obs: der synes at være forskel på strålefølsomhed hos gr. II (fravær af histopatologisk nekrose medfører bedre følsomhed)
- Kemoterapi: Bør foregå protokolleret. Se også afsnit 7.7 om medicinsk antineoplastisk behandling.
- Opfølgning: MR skanning efter 3 måneder, herefter 9 mdr, 15 mdr, 2 år, 3 år, 5 år, 7 år og 10 år. Ved inkomplet resektion bør 48 timer MR foretages. (recidiv rate på 5 år er 30 % ved GTR og 40 % på STR)
Meningeom grad 3
- Er karakteriseret ved invasiv vækst i cortex, høj recidiv risiko og kan metastasere systemisk.
- Behandling: GTR er målet efterfulgt af RT 54 Gy på 1,8 -2,0 /fraktion. (Ved mistanke præ- eller peroperativ bør 48 timers kontrolskanning overvejes af hensyn til efterfølgende strålebehandling).
- Opfølgning: Første gang efter behandling 3 måneder, herefter hver 3 - 6 måned afhængig af vækst potentiale.
- 5 års PFS er mellem 12 og 75 % trods kirurgi og SRT.
- Kemoterapi: Bør foregå protokolleret.
Literatur
--Jannick Brennum 1. apr 2018, 18:07 (UTC)