Gliomer
Indledning
Gliomer er tumorer (omer) der stammer fra hjernens støttevæv = glia. De hyppigste glia celler danner tumorer er astrocytter der bliver til astrocytomer, oligodendrocytter der bliver til oligodendrogliomer og ependymceller der bliver til ependymomer. Gliavævet fornyes hele livet igennem ligesom de fleste andre celler i kroppen i modsætningen til nervecellerne i hjernen (neuronerne) hvor der i voksen livet kun er meget sparsom eller sket ingen nyproduktion. Derfor ses der hos voksne ikke tumorer der stammer fra neuronerne. Der er forskellige teorier om oprindelsen af gliomer, du kan læse mere om dette i artiklen Stamceller og gliomer.
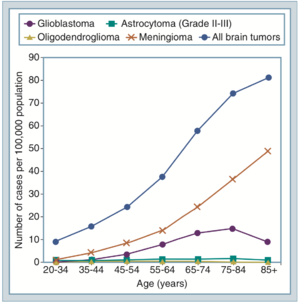
Som det ses af figur 1 er gliomer sjældnere diagnostiseret end meningeomer - og det ses endvidere at for næsten alle tumorer der ikke er specifikke børnetumorer ses de med øget hyppighed med stigende alder.
Epidemiologi
Gliomer udgør ca. 28% af alle hjernetumorer men 80% af det samlede antal af maligne hjernetumorer. Der har været en jævn vækst i antallet af gliomer diagnostiseret gennem de sidste 3 dekader, dette skyldes formodentlig primært 2 forhold. Dels har vi fået betydeligt bedre billeddiagnostik med langt større tilgængelighed, dels har vi en stigende ældre befolkning og vi er i denne periode blevet langt mere aktive i udredning og behandling af ældre.
Incidensen af gliomer er på verdensplan ca. 6/100.000/år.
Mænd har en højere hyppighed af gliomer end kvinder.
Ætiologi
Der er fundet end lang række faktorer der øger (+) eller reducerer risikoen for at udvikle gliomer (-):
- Højdosis strålebehandling (+++)
- Mandligt køn (+) specifikt for glioblastomer
- Neurofibromatosis type 1 (+++) astrocytomer
- Neurofibromatosis type 2 (+++) ependymomer
- Tuberøs sklerose (+++) astrocytomer og ependymomer
- Lynch’s syndrom (+++) astrocytomer
- Li-Fraumeni syndrom (+++) mest for glioblastomer
- Melanoma-astrocytom syndrom (+++)
- Ollier’s sygdom/Maffucci’s syndrom (+++)
Inherited single nucleotide polymorphisms rs1920116-C (TERC)
rs2736100-G (TERT), rs2252586-T (EGFR), rs11979158-A (EGFR), rs55705857-G (CCDC26), rs1412829-C (CDKN2B), rs498872-T (PHLBD1), rs78378222-C (TP53), rs6010620-G (RTEL1)
Mulige risiko faktorer
- Allergi/asthma (-)
- Lang telomer længde (+)
- Forhøjet immunglobulin E (-)
- Antistoffer mod variecella - zoster (-)
I et studie af 500 gliom patienter fandt man arvelig disposition hos mindre end 1% (Wensch et at 1997)
Histologi
Den seneste WHO-klassifikation er fra 2016. I denne klassifikation i forhold til de tidligere har molekylær genetiske undersøgelse fået en langt fremtrædende plads. En af de meget væsentlige forhold er skelnen mellem astrocytomer og oligodendrogliomer molekylær genetisk hvor den almene histologisk vurdering er trådt i baggrunden. Dette er et gennembrud, da der tidligere var stor forskel mellem patologiske laboratorier i vurderingen af den samme vævsprøve, og endvidere har det betydet af blandingstumoren Oligo-Astrocytom helt er udgået. Jeg forventer at dette dels betyder væsentlig større homogenitet i klassifikationen af gliomer, dels at vores prognostiske forudsigelse bliver mere præcise. Ved re-analyser af væv fra fra før de nye klassifikation ses det at prognosen for oligodendrogliomer er bedre end tidligere antager.
Gliom grader
- WHO Grad I = benigne
- WHO Grad II (lavgrads gliomer)- lang de fleste grad II gliomer vil på et eller andet tidspunkt udvikle sig til højgrads gliomer, hyppigere og hurtigere for astrocytomer end oligodendrogliomer.
- WHO grad III - IV = maligne (højgrads gliomer). Grad III kaldes oftest anaplastisk, grad IV: glioblastoma multiforme.
MOLEKYLÆR GENETISKE MARKØRER
- IHD(1 eller 2) mutation: ved grad 2 & 3 cytomer og oligodendrogliomer
- Codeletion med komplet tab af begge kromosomarme 1p/19q: Oligodendrogliomer
- Histone H3-K27M mutation: Diffuse midtlinje hjernetumorer
- MGMT promotor methylering: Medfører større effekt af kemoterapi
- Manglende ATRX ekspression: Foreneligt med IDH-muteret astrocytom uden 1p/19q deletion
Symptomer
Symptomer afhænger af tumors lokalisation, men overordnet kan de inddeles i 3 kategorier:
- Lokal dysfunktion: Disse symptomer skyldes at tumor komprimerer hjernen samt det nogle gange meget betydelige ødem omkring tumor. Fokale symptomer er helt afhængige af tumors lokalisation, fx ændret psykisk adfærd ved store olfactorius meningeomer. Et sjældnere men differentialdiagnostisk vigtigt symptom er supranukleære paraparesis inferior ved falx meningeom som komprimerer begge mesiale frontallapper sv.t. benets motoriske cortex, dette kan forveksles med eksempelvis cervikal stenose.
- Irritative symptomer: Lang det hyppigste irritative symptom ved meningeomer er epilepsi, for praktiske formål kun ses ved de supratentorielle meningeomer. Smerte ses nogle gange unden større masseeffekt, dette skyldes formodentligt den lokale irritation af dura.
- Tryksymptomer: Hovedpine, kvalme og opkastninger. Tumorer der obstruerer CSF flow som eksempelvis ved kompression af IV-ventrikel i fossa posterior medfører hydrocephalus, som kan give tryksymptomer.
Billeddiagnostik
MR og efterhånden i mindre grad CT er de væsentligste undersøgelse i udredningen af hjernetumorer. CT-skanning af hjernen anses i dag ikke som værende tilstrækkelig men det er MR oftest, hvorfor CT i stigende grad undlades. MR-skanning foretages med og uden kontrast (T1-vægtede billeder), hvor kontrastopladning i tumor er karakteristisk for højgrads gliomer men ikke specifikt for dem. Skanning udføres med tynde snit så de kan anvendes til neuronavigation ved kirurgisk indgreb. Som minimum udføres endvidere FLAIR og T2-vægtede billeder. I stigende grads udføres andre sekvenser som diffusions-vægtede billeder og blod-volumen billeder da disse kan indikerer malignitetsgraden af tumor.
PET-skanning, anvendes i stigende grad til vurdering af tumor udbredning, skelnen mellem tumorvæv og reaktive forandringer efter tidligere kirurgi, samt identifikation af "hostspots" som kan lokalisere mere maligne områder af tumor til brug for biopsier.
DTI-tractografi anvendes til at fremstille nervebanerne i hjernen, de kan være en stor hjælp ved planlægning af kirurgi.
fMRI kan anvendes til kortlægning af funktioner på hjernens overflade, vi anvender det ikke så oftest anvender vågen operation med mapping når tumor er lokaliseret tæt på vigtige = elokvente funktioner
Vigtigste differentialdiagnostiske overvejelser er for lavgradstumorer:
- infarkt & encephalitis.
For højgradstumorer:
- metastase & absces
Prognostiske faktorer
- Histologi
- Alder
- Funktions niveau
- Præoperative neurologiske udfald
- Resektionsgrad ved kirurgi
- Følsomhed for kemoterapi (MGMT promotor methylerings status)
Resektionsgrad som betydende faktor for overlevelse har været meget diskuteret gennem tiden, men i de senere år er der generelt enighed om at dette er en meget betydende faktor. Flere forhold har hjulpet, primært indførelse af tidlig postoperativ kontrol MR-skanning inden for 72 timer efter operationen, har givet et langt tydeligere billed af hvor meget tumor der fjernes end tidligere tiders vurdering af kirurgen. Efter indførelse af 5-ALA fluorescein ved resektion af maligne gliomer overraskes kirurger over hvor meget mere udbredt tumor er end når der blot anvendes normalt hvidt lys i operationsmikroskopet.
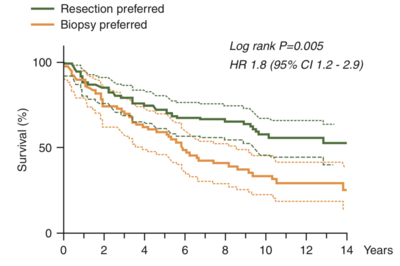
Der er kun få og små randomiserede kontrollerede studier af kirurgiens betydning og langt de fleste studier er retrospektive. Et studie af effekten på lavgrads gliomer fra Norge er dog særligt overbevisende. Her sammenlignede man overlevelse for lavgrads gliomer mellem to samtidige grupper af patienter behandlet på 2 forskellige neurokirurgiske afdelinger, hvor den ene afdeling stræbte efter så radikal fjernelse af tumor som muligt, mens den anden afdeling typisk undlod reaktion og blot foretog en biopsi (Jakola et al 2017). Dette var to helt rimelige valg, da der på det tidspunkt ikke var god evidens for eller i mor kirurgisk behandling. I figur 3 ses overlevelses kurverne for patienterne fra hver af de to afdelinger med en overbevisende effekt af kirurgisk behandling.
Behandling
Kirurgi
En arbejdsgruppe bestående af neurokirurger, onkologer, radiologer, patologer med flere (Danish Brain Tumour Study Group), har anbefalet følgende indikationer for operation af primære hjernetumorer:
- Tilsigtet helbredelse
- Forlængelse af patientens liv
- Udsættelse af udvikling af nye symptomer
- Lindring af fokalt symptom
- Lindring af symptomer på forhøjet intrakranielt tryk
- Diagnostisk
Følgende forhold kan have indflydelse på stillingtagen til operation:
- Tumors beliggenhed og den dermed forbundne risiko for neurologiske udfald i forbindelse med operativt indgreb.
- Patientens almene tilstand.
- Medicinske komplicerende faktorer.
- Patientens og de pårørendes ønske. Dette skal ses på baggrund af de fleste gliompatienters generelt dårlige prognose og de begrænsede behandlingsmuligheder (se nedenfor).
Ved recidiv er operationen palliativ, og indikationen afhænger så ledes af patientens symptomatologi. Det kan også dreje sig om at bekræfte malign degeneration af tumor, i hvilke tilfælde kemoterapi kan tilbydes (se nedenfor).
Radikalitet kan som regel kun afgøres ved en tidlig (mindre end 72 timer) postoperativ MR-skanning.
Ved operation kan man ved maligne gliomer tydeligere skelne patologisk fra ikke patologisk væv, end når det drejer sig om lavgradsgliomer. Imidlertid er reel kirurgisk radikalitet sjældent eller aldrig mulig, da der altid vil være ikke synlige tumorceller uden for det makroskopisk synlige tumorområde. Kun ved grad 1 gliomer og muligvis enkelte grad 2 gliomer er egentlig radikalitet mulig. Da der sandsynligvis kan opnås forlænget symptomfrihed og overlevelse ved fjernelse af al makroskopisk synligt tumorvæv (makrototal fjernelse), anbefales dette for tumorer, som ligger i ikke elokvente områder. Det er op til kirurgen om der anvendes sårdræn (subgalealt dræn), når det anvendes skal det fjernes dagen efter operationen.
Postoperativt behandlingsregime
- Principielt kan patienten straks mobiliseres og bør mobiliseres senest dagen efter operationen. Efter drænfjernelse er kun en mindre forbinding, eventuelt slet ingen nødvendig.
- Smertebehandling: smerter er sædvanligvis ikke et stort problem i den postoperative periode. Normalt ordineres til lige efter operationen paracetamol 1 g x 4 og morfin 2½-10 mg p.n., naturligvis under hensyntagen til patientens størrelse samt risiko for respirationsdepression.
- Patienten tilses senest ved aftenstuegang af vagthavende læge med henblik på bevidsthedsniveau og nytilkomne neurologiske udfald. Det skal registreres i journalen, om patienten er vågen, med/uden neurologiske udfald. Langt de fleste postoperative hæmatomer opstår inden for de første 6 timer efter operationen og vil oftest føre til en akut eller subakut forværring af den neurologiske status. Akut CT/eventuel operation er da nødvendig.
- Ved førstegangsoperation fjernes trådene 6. dagen efter operationen. Hvis patienten har fået steroider i mere end 10 døgn inden operationen, eller hvis der er tale om reoperation, fjernes trådene 8. dagen.
- Er der foretaget en god dekompression ved operationen kan steroidbehandlingen som regel aftrappes ret hurtigt, og hvis patienten kun har fået prednison i et par uger, kan aftrapningen foregå i løbet af få dage, da der endnu ikke er sket en binyrebark-suppression.
Komplikationer til kirurgi
Komplikationer til kirurgi kan opdeles i standars komplikationer hvor risikoen for såvel post-operativ blødning der kræver ny operation som infektion, normalt angives til hver ca. 1%. Risikoen for nye neurologisk udfald afhænger helt af tumors lokalisation. Andersen af ny udfald er langt størst umiddelbart efter operationen dels på grund af reaktivt ødem og iskæmi i resektionskanten, dels fordi pga. effekten af neuroplasticitet i tiden efter operationen hjulpet af træning. Det er svært at giver generelle risici for nye neurologiske og kognitive udfald, men disse undervurderes generelt, specielt når det drejer sig om milde og moderate udfald (Brennum et al 2018). Alle neurologisk og kognitive udfald bør ikke ses som en komplikation men som en nødvendig følgevirkning af operationen for at opnå en høj grad af resektion og dermed forlænget overlevelse. Kirurgen må før operationen drøfte denne afvejning af potentielt tab af funktion overfor livslængde, den såkaldet onco-funktionelle balance.
Onkologisk efterbehandling
- Efterbehandling tilbydes som regel kun patienter i WHO performance status 0-2 (svarer til, at 50% af tiden tilbringes uden for sengen). Dårligere pt. kan evt. tilbydes “palliativ” strålebehandling (5 Gy x 4). Strålefeltet omfatter tumor + 2cm ekstra
- Grad I tumorer: ikke indikation for efterbehandling.
- Grad II tumorer: normalt ikke indikation for postoperativ strålebehandling. Strålebehandling kan tilbydes senere ved “recidiv” ;. Strålebehandlingen er 44 Gy med 2,0 Gy per fraktion/varighed ca. 4½ uge.
- Grad III-IV gliomer: patienter <70 år: Postoperativ strålebehandling 60 Gy med 2,0 Gy per fraktion/varighed 6 uger. Denne behandling kalder onkologerne “kurativ”.
- Kemoterapi: Temozolamid er standardbehandling i kombination med strålebehandlingen ved Glioblastomer. Patienter med maligne oligodendrogliomer får dog fortsat som tidligere cis-platin, etoposid og BCNU. Temozolamid (temodal)-behandling gives i tabl.form, og behandlingen kan foregå ambulant.
- Hvis der er forsøgsbehandling, tilbydes patienter eventuelt at indgå i protokollen.
- Ved recidiv efter strålebehandling drøftes patienten på MDT-konference hvor: Reoperation, anden kemoterapi & eksperimentelle behandlingsprotokoller overvejes.
- Stereotaktisk radiokirurgi er stort set aldrig indiceret ved primære hjernetumorer.
- Henvisning til onkologisk afdeling sendes som Best.Ord. i SP, så snart frysehistologisk svar foreligger, typisk samtidigt med operationsbeskrivelsen.
- Fysiurgisk efterbehandling/optræning tilbydes afhængig af den neurologiske status og sygdommens prognose.
- GOP = Genoptrænings plan tilbydes til patienter der ikke overflyttes til lokal neurologisk afdeling
Andet
Immunterapi Der forskes meget i immunterapi men det har endnu ingen plads i rutine behandling. Hjernen betragtes som et "koldt" immunologisk område og endnu har der kun været påvist sporadisk effekt.
Elektrisk stimulation tumor treating fields (TTT) er en nyere behandling hvor patienten behandles med elektrisk strøm på hovedet via elektroder der er sat på hovedet med plaster. De foreløbige studier tyder på at der er nogen effekt (Mittal et al. 2018)
Literatur
- Jakola, AS, Skjulsvik, AJ, Myrmel, KS, Sjåvik, K, Unsgård, G, Torp, SH, Aaberg, K, Berg, T, Dai, HY, Johnsen, K, Kloster, R, Solheim, O. Surgical resection versus watchful waiting in low-grade gliomas. Ann Oncol 2017;28:1942-1948.
- Kræftens Bekæmpelses hjemmeside: [cancer.dk]
- Mittal, S, Klinger, NV, Michelhaugh, SK, Barger, GR, Pannullo, SC, Juhász, C. Alternating electric tumor treating fields for treatment of glioblastoma: rationale, preclinical, and clinical studies. J Neurosurg 2018; 128, 414-421.
- Youmans Neurological Surgery, 7th edition 2017
- Weller, M, van den Bent, M, Tonn, JC, Stupp, R, Preusser, M, Cohen-Jonathan-Moyal, E, Henriksson, R, Le Rhun, E, Balana, C, Chinot, O, Bendszus, M, Reijneveld, JC, Dhermain, F, French, P, Marosi, C, Watts, C, Oberg, I, Pilkington, G, Baumert, BG, Taphoorn, MJB, Hegi, M, Westphal, M, Reifenberger, G, Soffietti, R, Wick, W, European, AFN-OEANOTFOG European Association for Neuro-Oncology (EANO) guideline on the diagnosis and treatment of adult astrocytic and oligodendroglial gliomas. Lancet Oncol 2017;18, e315-e329.
- Wrensch M, Lee M, Miike R, et al. Familial and personal medical history of cancer and nervous system conditions among adults with glioma and controls. Am J Epidemiol. 1997;145:581-593.
--Jannick Brennum 2. apr 2018, 12:11 (UTC)