Svær bevidsthedssvækkelse, konfusion og delir
Baggrund
Der har været et ønske fra personalet i Neurokirurgisk Klinik på Rigshospitalet om at få udarbejdet en tekst, der kan introducere personalet til fænomenerne svær bevidsthedssvækkelse og konfusion/delir som et supplement til den undervisning om emnerne, der regelmæssigt gives af neuropsykologerne i klinikken. Afsnittene om henholdsvis Begrebsafklaring og Behandling/rehabilitering/tiltag er umiddelbart særligt relevante for sundhedspersonale. Hvis du/I har spørgsmål eller kommentarer til nærværende tekst, så kontakt venligst neuropsykolog Christina Engelmann, der har udarbejdet den. Teksten er et internt arbejdspapir til Neurokirurgisk Klinik, men andre er velkomne til at bruge teksten, såfremt der refereres til, hvor og hvem de har den fra.
Historisk set
Vi skal mindre end hundrede år tilbage, førend der begynder at komme mere anvendelige operationelle definitioner på bevidsthedsbegrebet. Eksempelvis blev hjernedødsbegrebet (først) introduceret i begyndelsen af 1950’erne. Dette i forbindelse med poliomyelitis-udbruddet i Danmark i 1952, hvor knap 3000 mennesker udviklede sygdommen over en periode på 6 måneder, hvoraf en stor del af disse også udviklede luftvejslammelser. Anæstesilæge Bjørn Ibsen iværksatte på daværende tidspunkt manuel ventilering af patienterne på det daværende Kommune Hospital i København med hjælp fra flere hundrede medicinstuderende, hvilket fik dødeligheden til at falde markant. Herved blev dødsbegrebet/hjernedødsbegrebet redefineret ud fra neurologiske kriterier. I 1953 grundlagde Bjørn Ibsen den første respiratorbehandling og den første egentlige intensivafdeling i Danmark og på verdensplan.
I 1966 udgav Plum & Posner bogen ”The Diagnosis of Stupor and Coma”, hvori Locked-In Syndrom (LIS) introduceredes.
I 1972 introducerede og omdefinerede Jennett & Plum begreberne Koma og Persistent vegetativ tilstand, og i 1974 publicereredes første artikel af Jennett & Teasdale om Glasgow Coma Scale (GCS). Denne skala blev oprindelig introduceret med henblik på at rate/vurdere ændringer i bevidsthedsniveau og/eller funktionsniveau hos patienter, der har været udsat for traumatisk hjerneskade (TBI), men skalaen vandt hurtigt indpas og er siden blevet anvendt til også at beskrive bevidsthedsniveau og/eller funktionsniveau hos alle andre neurologiske og neurokirurgiske patientgrupper.
Disse ”nye” begreber og GCS gav et nyt fælles sprog i beskrivelsen af mennesker med svær bevidsthedssvækkelse, men der blev ikke rigtig skelnet mellem årsag og patologi. Det var først i midten af 1990’erne, at der begyndte at komme mere fokus på at udforme operationaliserede begreber/definitioner, der kunne styrke klinikkere/forskere i forhold til, hvordan patienter med svær bevidsthedssvækkelse adskiller sig fra andre patienter, der er begrænsede i deres energiniveau og rettethed/fokusering og reaktion på omgivelserne.
Eksempelvis blev i 1994 introduceret begrebet Permanent vegetativ tilstand (PVS) af the Multi Society Task Force on PVS (inklusiv American Academy of Neurology (AAN)), og i 1997 blev begrebet Minimalt bevidsthedsniveau (MCS) introduceret af Aspen Consensus Group (første publikation ved Giacino et al, 2002), ligesom Aspen-kriterierne for svær bevidsthedssvækkelse blev introduceret. Aspen-kriterierne vil blive gennemgå nærmere i det følgende. Der har gennem tiden været flere forskningsfællesskaber omkring svær bevidsthedssvækkelse, herunder eksempelvis Coma Science Group anført af Steven Laureys (Liège, Belgien) som bl.a. har fokuseret en del på sammenhængen mellem de forskellige former for bevidsthedssvækkelse og billeddiagnostiske data. Coma Science Group introducerede endvidere i 2006 begrebet Functional Locked-In (LIS*) og i 2010 begrebet Unresponsive Wakefulness Syndrome (UWS). (http://www.coma.ulg.ac.be/)
Siden hjernedødsbegrebets indtog i 1950’erne er der således kommet flere begreber til, som vil blive gennemgået mere detaljeret i de følgende afsnit.
Begrebsafklaring
Der kan være mange medicinske årsager til, at et menneske bliver bevidsthedssvækket og/eller kommer i en konfusionstilstand. Ofte skyldes det en eller anden form for diffus cerebral påvirkning - eksempelvis som følge af TBI eller ikke-traumatisk hjerneskade (non-TBI) (fx subaraknoidalblødning, hydrocephalus, infektion, forgiftning, anoksi, metaboliske sygdomme, medicinpåvirkning etc.), som bl.a. medfører ubalance i den cellulære metabolisme (hjernens stofskifte) og derved reduktion i den globale cerebrale synaptiske aktivitet. Jeg vil i det følgende sidestille den danske betegnelse svær bevidsthedssvækkelse med den engelske Disorders of Consciousness (DOC).
Det er vigtigt at pointere, at svær bevidsthedssvækkelse ikke er det samme som Locked In Syndrom (LIS), der skyldes en isoleret påvirkning på hjernestammeniveau (skade af de kortikospinale og de kortikobulbære baner), og som ikke umiddelbart giver bevidsthedspåvirkning, men derimod giver svære motoriske problemer i form af lammelse af de fleste muskelgrupper i kroppen, herunder ingen eller ganske sparsom forbindelse mellem hjernen og kroppens muskler (medfører aphoni og tetraplegi). Ved klassisk LIS vil det kun være muligt for personen at udføre blinken og vertikale øjenbevægelser, hvilket er meget begrænset bevægelse, men for nogle menneskers vedkommende tilstrækkelig bevægelse til at kunne kommunikere sikkert og nuanceret med omgivelserne. Nogle patienter med LIS vil dog være svært bevidsthedssvækkede i ”den akutte fase”, hvilket potentielt kan medføre fejldiagnosticering, herunder også misforståelser i kommunikationen med patienten.
Man har i mange år anvendt forskellige ord for grader af bevidsthedssvækkelse eller bevidsthedspåvirkning (fx coma vigile, apallisk syndrom, stupor, somnolens eller andet), men midt i 1990’erne begyndte man i forskellige settings at revidere de diagnostiske kriterier for svær bevidsthedssvækkelse. I 1996 afholdt man eksempelvis en tværfaglig ”konsensus-konference” i Aspen/USA, hvor man opsummerede en stor del af den samlede viden på området og blev enige om, hvilke begreber der på den mest fyldestgørende måde beskrev de forskellige bevidsthedstilstande (Aspen Consensus Conference Work-Group - en samling af sundhedspersonale indenfor neurologi, neurokirurgi, neuropsykologi og rehabilitering). Der har siden da været udmeldinger om andre beskrivelser og diagnostiske kriterier, men indtil videre er det ”Aspen-kriterierne”, der har vundet indpas (Giacino et al, 2002, 2004, 2009; Giacino, 2005; Giacino & Whyte, 2005; Bernat, 2006; Laureys et al, 2010; Jox et al, 2012, Gosseries et al, 2014).
Ud fra Aspen-kriterierne inddeles svær bevidsthedssvækkelse i tre ”tilstande”: Henholdsvis koma, vegetativ tilstand og minimalt bevidsthedsniveau (beskrives nærmere nedenfor).
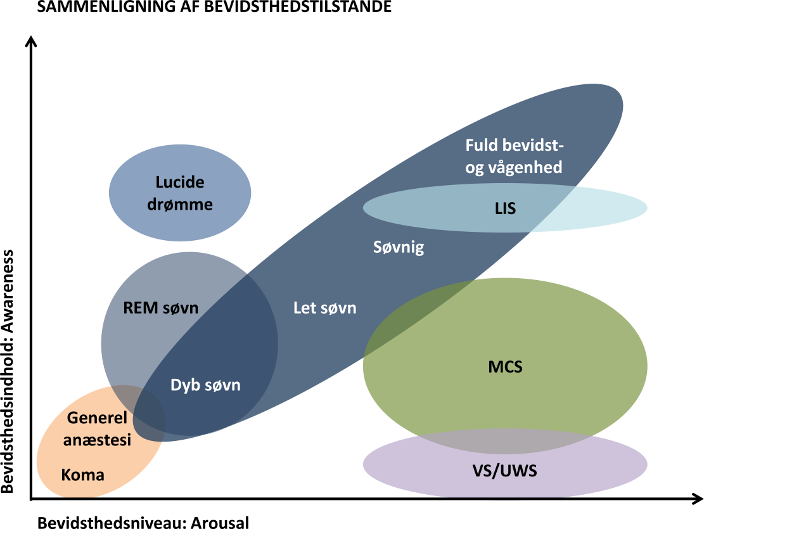
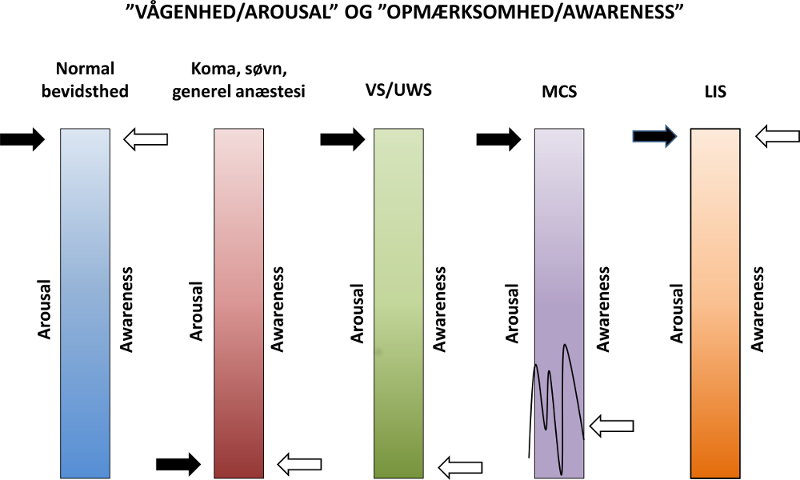
De enkelte tilstande kan på en forholdsvis enkel måde beskrives ud fra de engelske begreber arousal og awareness. Der findes ikke nogle helt dækkende ord for begreberne på dansk, men arousal har med vågenhed og energiniveau at gøre, og awareness har noget at gøre med bevidsthed om et givent emne eller en form for rettethed/fokusering af opmærksomhed mod sig selv eller omgivelserne – figur 1.
Figur 1 – tilpasset af neuropsykolog Jens Sommer fra Laureys et al, 2004, figur 2, side 538 http://www.coma.ulg.ac.be/papers/vs/PVS_MCS_LIS_LancetN04.pdf
Koma
Når en patient er i koma, er der hverken arousal eller awareness. Patienten ligger således med lukkede øjne og skal have hjælp til at trække vejret (ingen arousal), ligesom patienten heller ikke retter sin opmærksomhed mod sig selv eller omgivelserne – patienten reagerer ikke på, hvad der sker i dem eller omkring dem, eksempelvis følges verbale opfordringer om at trykke i hånd eller åbne munden (ingen awareness) ikke. Koma varer som oftest 2-4 uger, hvorefter patienten enten øger bevidsthedsniveauet (overgår til VS/UWS eller MCS) eller dør af den primære skade (Giacino et al, 2013).
Vegetativ tilstand (VS/UWS)
Når en patient er i den vegetative tilstand (VS), så er patienten som udgangspunkt i stand til at trække vejret selv (der kan være særlige årsager til, at dette ikke er muligt) og kan måske endda udvise en eller anden form for døgnrytme – eksempelvis have åbne øjne om dagen og lukkede øjne om natten (begyndende arousal). Patienten reagerer dog ikke på, hvad der sker i dem eller omkring dem - eksempelvis følger patienten ikke verbale opfordringer om at blinke, vise fingre, trykke i hånd, åbne munden eller andet (ingen awareness). Det skal tilføjes, at der er kommet flere forslag til nuancering af Aspen-kriterierne. I den forbindelse har specielt en forskningsgruppe skilt sig ud, nemlig den belgisk baserede forskningsgruppe Coma Science Group, ledet af Steven Laureys (www.coma.ulg.ac.be). De har foreslået, at man går væk fra begrebet VS, da det kan give nogle sproglige misforståelser og associationer til ”grøntsager”. Coma Science Group foreslår i stedet, at man anvender begrebet Unresponsive Wakefulness Syndrome (UWS) (Laureys et al, 2010) (eller på dansk ”Uresponsiv Vågenhedssyndrom” fra Gosseries et al, 2011). I det følgende vil jeg bruge begge begreber sidestillet, dvs., VS/UWS.
Det skal også tilføjes, at der har været en del begrebsforvirring omkring VS/UWS, specielt angående hvornår man kan kalde tilstanden for stationær. I 1972 præsenterede Jennett og Plum for første gang begrebet Persistent vegetativ tilstand (PVS) og beskrev det som en vågen form for koma. I 1982 omdefinerede Plum og Posner det til VS/UWS i længere tid, og i 1994 blev det af Multi Society Task Force on PVS (en sammenslutning af repræsentanter fra flere amerikanske lægefaglige selskaber, herunder American Academy of Neurology) besluttet, at Persistent vegetativ tilstand er et udtryk for, at en patient har været i VS/UWS over 1 måned uanset skadestype. Multi Society Task Force on PVS introducerede i 1994 også begrebet Permanent vegetativ tilstand (PVS), defineret ved, at VS/UWS har varet så længe, at bedring er usandsynlig, men dog ikke umulig, samt at varighed afhænger af skadestype (for uddybning se nedenfor under afsnittet om prognose). Aspen Consensus Conference Work-Group har opfordret til, at man ikke anvender begreberne persistent og permanent VS/UWS, da begreberne i deres ordlyd skønnes misvisende. Det er dog begreber, der stadig anvendes i litteraturen og i visse statistiske opgørelser. I den kliniske praksis i Danmark kan man i stedet overveje at være mere beskrivende i sin tilgang og eksempelvis anvende følgende beskrivelse: '”patienten har ud fra Aspen-kriterierne været i VS/UWS i 6 uger grundet TBI”' (Giacino & Schiff, 2009; Laureys et al, 2010; Owen et al, 2011; Gosseries et al, 2014).
Minimalt bevidsthedsniveau (MCS)
Når en patient er i/på minimalt bevidsthedsniveau (MCS), så er patienten som udgangspunkt i stand til at trække vejret selv (der kan igen være særlige årsager til, at dette ikke er muligt) og kan måske endda udvise en eller anden form for døgnrytme – eksempelvis åbne øjne om dagen og lukkede øjne om natten (”begyndende” arousal). Indimellem, men ikke altid, kan patienter ydermere reagere på, hvad der sker i dem eller omkring dem - eksempelvis følge verbale opfordringer om at blinke, udvise visuel følgen af bevægelse, vise fingre, trykke i hånd, åbne munden eller andet (begyndende, men ikke altid vedvarende awareness, hvor rettetheden/fokuseringen af opmærksomheden mod omgivelserne er inkonsistent).
Konfusionstilstand, herunder post-traumatisk amnesi for TBI-patienter
Når en patient 'konsistent' kan følge en simpel verbal opfordring eller vise anvendelse af to helt simple hverdagsting (eksempelvis en tandbørste, en ske, en kam etc.), så betragter man ikke længere patienten som svært bevidsthedssvækket, men nærmere som et menneske, der nu er ”overgået” til en konfusionstilstand. Ved konfusionstilstand forstås mennesker, der er '”usamlede i deres tænkning, adfærd og opfattelse af virkeligheden”' (Klinisk Ordbog, 2005).
Nogle vil skelne mellem konfusionstilstand og delir og andre vil mene, at det er to ord, der beskriver den samme tilstand. Ifølge klinisk ordbog (2005) dækker begreberne den samme tilstand:
- Confusio: ”(latin confusio sammenblanding, forvirring, uorden (latin confundo blander/roder sammen)) … usamlethed i tankegang, adfærd og i opfattelsen af omgivelserne … ofte ledsaget af desorientering …”.
- Delirium: ”(latin de bort fra + lire plovfure) … delirøs tilstand, konfusionstilstand: Tilstand med bevidsthedsuklarhed i form af nedsat opfattelse af omgivelserne og svækket opmærksomhed … kan ses i forbindelse med organiske hjernelidelser … ved forgiftning … og abstinenstilstand efter brug af psykoaktive stoffer …”.
I en akut konfusionstilstand kan arousal og awareness stadig variere (og endda også variere/fluktuere en del), således at patienten på nogle tider af døgnet kan fremstå meget træt og langsom (hypo-aktiv tilstand) og på andre tidspunkter fremstå ”overgearet”/motorisk urolig/”usamarbejdsvillig”/”agiteret” (hyper-aktiv tilstand).
Ved agitation forstås en ” … tilstand præget af øget psykomotorisk aktivitet med udtalt rastløs uro.” (Klinisk ordbog, 2005), og en ”Tilstand præget af øget motorisk aktivitet, der viser sig ved rastløs uro, i de sværeste tilfælde ved konstant formålsløs hyperaktivitet med omkringvandren, hændervriden, roden, pillen eller iturivende adfærd.” (Psykiatrisk ordbog, 2000). Det skal påpeges, at agitation ikke er det samme som aggression, da sidstnævnte nærmere må betragtes som en eller form for målrettet adfærd - ”fra latin aggressio 'bevægelse hen imod', af aggredi 'gå hen til, angribe‘” (Klinisk ordbog, 2005).
Agitation kan være et udtryk for, at der er tilkommet ”noget konkurrerende” (eksempelvis sult, tørst, forstoppelse, sår, smerter, epileptiforme fænomener, hydrocephalus, infektioner, medicinpåvirkning eller andet), men det kan også være et udtryk for bedring i den forstand, at patientens arousal-niveau er steget markant, men dog uden at awareness er fulgt med i samme grad. Agitation kan være upraktisk for både patienten, medpatienter, pårørende og personale, da patienten med den ofte formålsløse motoriske uro vil kunne hive fat i ting på og omkring sig, hvilket kan være uhensigtsmæssigt og endda farligt, ligesom patienten i den tilstand kan have endnu større udfordringer med at fastholde opmærksomheden. Agitation hos patienter, der er under opvågning efter TBI, kan medføre følelsesmæssig belastning og nedsat livskvalitet hos pårørende (Norup et al, 2010). Der findes 'ingen' specifik behandling for agitation, men noget tyder på, at kognitiv bedring mindsker risikoen for agitation (Bockbrader, 2015), ligesom behandling af konkurrerende sygdomme kan mindske risikoen for agitation, herunder også fokus på at genvinde døgnrytme og mindske irrelevante stimuli (Bogner et al, 2015).
Det er velkendt, at arousal-niveauet (og derved risikoen for agitation) kan stige yderligere, hvis døgnrytmen er forstyrret, omgivelserne er støjende, og hvis patienten befinder sig i et miljø med mange og for patienten skiftende irrelevante stimuli (Grosswasser, 1996).
Det er også værd at nævne, at nogle patienter i en periode vil udvise en tendens til at putte ikke-spiselige ting i munden og måske endda synke dem, hvilket igen kan være upraktisk og i sidste ende også uhensigtsmæssigt og farligt. Fænomenet betegnes Pica (af latin pica 'skade, efter denne fugls tilbøjelighed til indsamling af uspiselige genstande' - fra Psykiatrisk Ordbog, 2000).
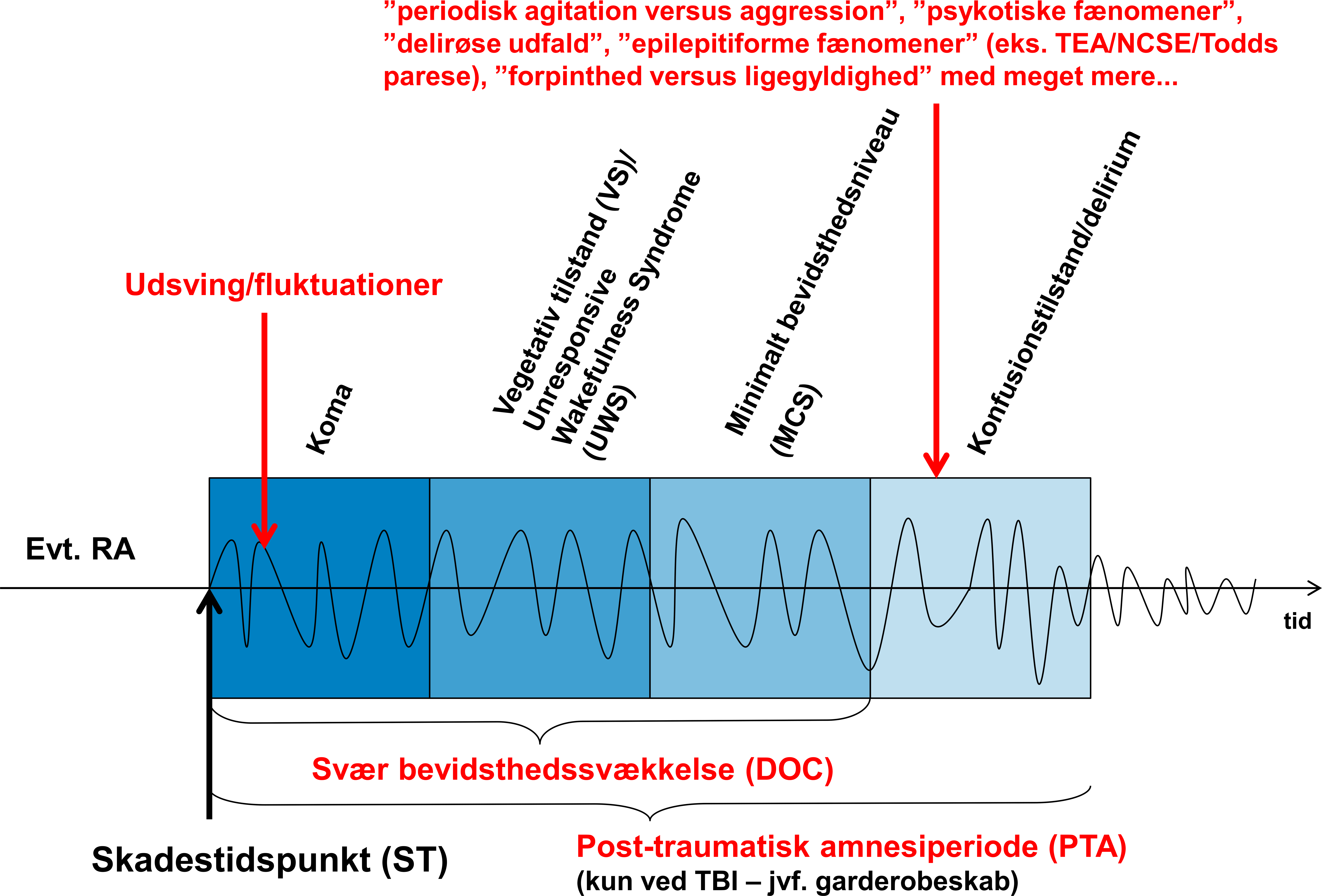
I en konfusionstilstand vil de fleste kognitive funktioner ofte være påvirkede, men specielt vil patientens ”opmærksomhedsfunktioner” være påvirkede – patienten vil afledes hurtigt og have svært ved at fastholde opmærksomheden i længere tid ad gangen (Corrigan et al, 1992; Wilson et al, 1999; Stuss et al, 1999; Bode, 2000; Nakase-Thompson et al, 2004; David et al, 2009) – figur 2. Patienten vil ofte være desorienteret (eksempelvis ikke være orienteret i hvem han/hun er, hvor han/hun er henne, hvilken dato det er, hvad der er sket med ham/hende, hvor længe han/hun har været her, hvem personalet er, hvem pårørende er med meget mere). Nogle patienter vil have amnesi (hukommelsestab) siden skaden (kaldes anterograd amnesi (AA)), andre vil have enkelte perioder af amnesi, og atter andre vil kunne huske alt fra skadestidspunktet. Nogle patienter vil have amnesi for episoder/hændelser op til skaden (retrograd amnesi (RA)), måske endda adskillige år før denne, og andre vil kunne huske alt op til skaden. Hvis patienten med tiden bliver mere orienteret og måske endda genvinder en sammenhængende hukommelse for begivenheder fra dag til dag, så vil den retrograde amnesiperiode ofte i takt med bedring blive mindre og mindre. Ikke sjældent kan en patient have en retrograd amnesiperiode på 10 år umiddelbart efter skaden, og senere hen i forløbet i takt med bedring, så vil det måske blot dreje sig om minutter/timer/dage. Længden af den retrograde amnesiperiode har ingen sammenhæng med prognose.
Figur 2 – udarbejdet af neuropsykolog Christina Engelmann
- Ved konfabulation forstås ”Beretninger uden hold i virkeligheden, hvormed patienter med hukommelsessvigt udfylder erindringslakuner” (Klinisk Ordbog, 2005).
- Ved reduplikativ paramnesi forstås ”Overbevisningen om, at personer eller ting findes i dubletter, som er fuldstændig ens eller ligner hinanden. Vrangforestillinger om personer med dobbeltgængere kaldes Capgras syndromet, og reduplikativ paramnesi er den tilsvarende vrangforestilling om, at et hus eller hospitalet er en replika eller kopi af det sted, hvor alle andre mener at befinde sig.” (Gads Psykologileksikon, 3. udgave, 2010).
For patienter, som har været udsat for traumatisk hjerneskade (TBI), kaldes perioden fra skadestidspunkt, til patienten har en sammenhængende hukommelse for begivenheder fra dag til dag for Post-Traumatisk Amnesi (PTA) (Russel et al, 1932; Symmonds et al, 1943; Russel et al, 1946; Russel et al, 1961; Ahmed et al, 2000) – figur 3. Denne periode kan variere fra sekunder til mange måneder, og nogle mennesker kommer aldrig ud af PTA, men vil vedblive at være i en konfusionstilstand, hvor de ikke husker tingene fra dag til dag (eksempelvis Forrester et al, 1994; Wilson et al, 1999). Måske vil de med tiden kunne lære nye procedurer (eksempelvis brygge kaffe på en ny kaffemaskine), men de vil ikke kunne huske, hvem de har fået kaffemaskinen af, eller hvornår de har fået den. Man kan være så fræk at sammenligne tilstanden lidt med ”et mentalt garderobeskab med rod i”. Når man skal indlære og senere huske noget, så skal man til at begynde med lægge tingene ind på de rette mentale hylder/skuffer eller hænge det på de rette bøjler. Når man kommer svært til skade, så vil erindringerne, eller de mentale hylder, skuffer og bøjler, være rodet sammen og ligge i en stor bunke – forstået på den måde, at patienten i yderste konsekvens ikke er orienteret i hvem de er, hvor de er henne, hvad der er sket, ligesom tidsfornemmelsen vil være forstyrret. I takt med, at der (for mange) sker fremgang, vil der gradvist (eller for nogle pludseligt) opstå bedring, således at patienten genvinder orienteringen, ligesom den i konfusionstilstanden ofte mangeartede kognitive påvirkning vil komme til udtryk i mere specifikke kognitive vanskeligheder. Det skal dog også nævnes, at der hos nogle patienter vil være forholdsvis få (eller måske endda ingen målbare) kognitive følgevirkninger, hvilket kan være en stærk kontrast til patientens adfærd i konfusionsperioden. Mennesker, der udsættes for penetrerende læsioner af hjernen (eksempelvis efter skudlæsioner, søm fra sømpistoler eller lignende), vil grundet den i højere grad ”fokale påvirkning” ikke nødvendigvis være i PTA efterfølgende (Mckinlay & Watkiss, 1999).
Figur 3 – udarbejdet af neuropsykolog Christina Engelmann
Opsummering, begrebsafklaring
De forskellige bevidsthedstilstande kan opsummeres ved følgende tekst samt i figur 4 og figur 5:
- Koma
(Ingen arousal eller awareness – lukkede øjne, ingen opmærksomhed mod omverdenen).
- Vegetativ tilstand (VS/UWS)
(Genvindelse af nogen arousal, ingen awareness - indimellem åbne øjne, eventuelt døgnrytme, ingen opmærksomhed mod omverdenen).
- Minimalt bevidsthedsniveau (MCS)
(Genvindelse af nogen awareness - inkonsistent/glimtvis rettethed/opmærksomhed mod omgivelserne, herunder visuel følgen af bevægelse, kommunikation og/eller funktionel objektbrug).
- Konfusion/delir
(Desorientering, flygtig opmærksomhed mod omgivelserne, usamlethed i tankegang, ofte manglende sammenhængende hukommelse for begivenheder fra dag til dag, eventuel hypoaktiv/hyperaktiv tilstand).
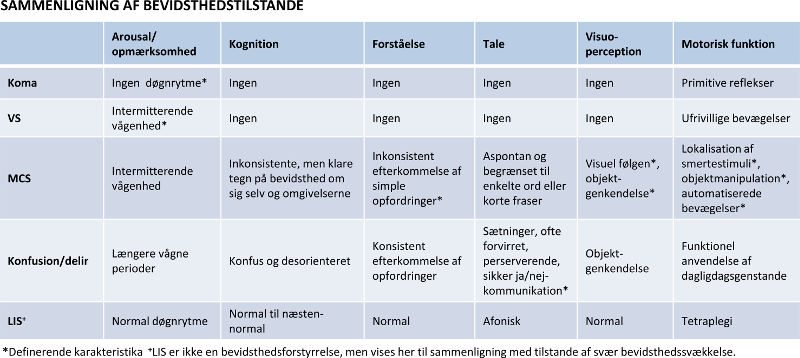
Figur 4 – tilpasset af neuropsykolog Jens Sommer fra Giacino et al, 2014, tabel 1, side 3
Figur 5 – tilpasset af neuropsykolog Jens Sommer fra Laureys, Scientific American, 2007, figure side 34 og 35 http://www.coma.ulg.ac.be/papers/vs/sci_am_07.pdf
Prognose
Uanset årsagen til bevidsthedssvækkelsen og/eller konfusion/delir, så kan man stagnere på alle niveauer. Der er forskellige opvågningsforløb fra skadestype til skadestype og fra person til person. De statistiske opgørelser fortæller som udgangspunkt noget om populationer (grupper af mennesker) og ikke noget sikkert om det enkelte individ. Når et menneske udsættes for cerebral påvirkning, så vil skaden og årsagssammenhængene således som udgangspunkt være multifaktorielle, og prognosen vil afhænge af blandt andet patientens alder på skadestidspunktet, årsag/ætiologi, varighed af aktuelle tilstand, sekundære følgevirkninger, aktuelle (konkurrerende) sygdomme med meget mere (Kraus et al, 1999; Graham et al, 1999).
Der er lavet flere studier om sammenhængen mellem svær bevidsthedssvækkelse og TBI end svær bevidsthedssvækkelse og andre årsager (non-TBI). Det tyder på, at ”vinduet for bedring” står åbent i længere tid for svært bevidsthedssvækkede patienter, der har været udsat for TBI, i forhold til patienter, der har været udsat for non-TBI (Giacino & Kalmar, 2005; Giacino et al, 2015) – figur 6.
Figur 6 – tilpasset af neuropsykolog Jens Sommer efter Giacino & Kalmar, 2005, tabel 1, side 171. Vær opmærksom på, at permanent vegetativ tilstand er defineret som, at nu har patienten været i VS/UWS så længe, at bedring er usandsynlig men ikke umulig
Man har gennem tiden forsøgt at forudse outcome ud fra forskellige parametre (eksempelvis Bishara et al, 1992; Katz og Alexander, 1994; Ellenberg et al 1996; Asikainen et al,1998; Brown et al, 2005; Engberg et al, 2006; Liebach et al, 2007, Sherer et al, 2008; Sidaros 2007/2009; Nakase-Richardson et al, 2011). Billeddiagnostiske analyser såsom EEG, CT og MR har imidlertid hidtil ikke sikkert vist sig at kunne forudsige outcome. Tidlig Glascow Coma Score har ej heller vist sig sikker, herunder er der også en stor usikkerhed omkring måletidspunkt, sedering og andet. Længden af bevidsthedstab (”time to follow command”) har imidlertid vist sig at være en rimelig prediktor i forhold til outcome hos patienter, der har været svært bevidsthedssvækkede i en længere periode (uger til måneder) – figur 7. Det er dog ikke umuligt, at et menneske (der har været udsat for TBI) opnår øget awareness mange år efter skadestidspunktet, hvilket kan betegnes som late recovery. Det er ekstremt sjældent, men det er ikke umuligt over tid at genvinde øget grad af selvhjulpenhed, kommunikative færdigheder, øget grad af orientering med mere over år. De late-recovery-cases, der er beskrevet hidtil, er alene baseret på TBI-patienter, og der er ingen patienter, som tilnærmelsesvis er kommet tæt på tilstanden før skaden.
Figur 7 – tilpasset af neuropsykolog Jens Sommer fra Asikainen et al, 1998
For mennesker, der har været udsat for TBI, og ikke har været svært bevidsthedssvækkede eller blot har været bevidsthedssvækkede i forholdsvist kort tid, der vil længden af PTA være den bedste prognostiske faktor – figur 8 og figur 9. Der er imidlertid stor uenighed om, hvor længe PTA skal vare, førend der er tale om svære følgevirkninger (se forskelle mellem figur 7, 8 og 9), og igen skal man være opmærksom på usikkerheden i at overføre statistisk materiale direkte til det enkelte patientforløb. Det ses ikke sjældent, at patienter, der blot kortvarigt har været i PTA, kan have omfattende fysiske, kognitive og/eller adfærdsmæssige forstyrrelser, ligesom en patient, der har været i PTA i længere end 28 dage eller lignende, på længere sigt kan genvinde et funktionsniveau, der er tæt på (og på nogle områder måske endda bedre) end før skaden. Igen er det multifaktorielt, og prognosen afhænger af, hvem der bliver ramt af hvad, hvordan og hvornår i deres livsforløb. Heraf følger, at det på baggrund af vores faktuelle viden og erfaring i dag ikke er muligt at udtale os sikkert om prognosen i den akutte fase.
Figur 8 – tilpasset af Jens Sommer fra Jennett & Teasdale, 1982
Figur 9 – tilpasset af neuropsykolog Jens Sommer fra Fleminger, 2009, tabel 4.3, side 188 (baseret på data fra Steadman & Graham; Greenwood, 2002)
Differentialdiagnostik
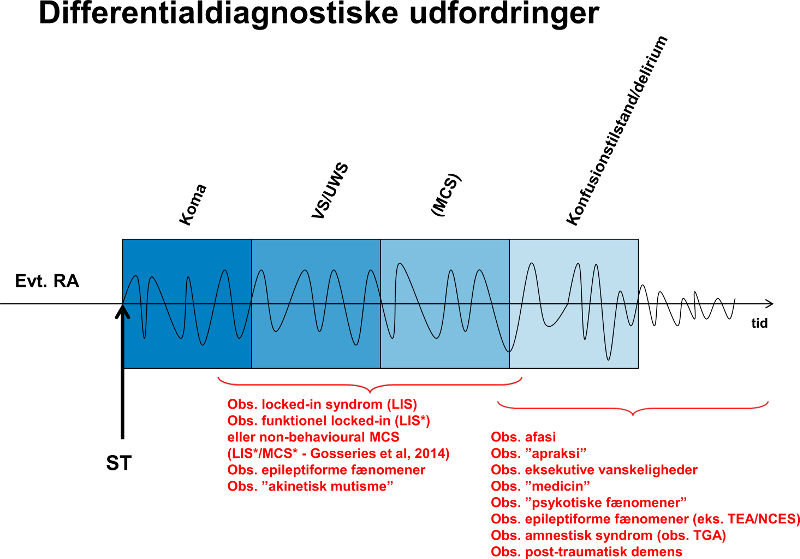
Svær bevidsthedssvækkelse og konfusion/delir kan være svære størrelser at skelne fra andre tilstande (figur 10), ligesom der ikke er opnået enighed om, hvornår vi skal begynde at kalde tilstandene noget andet. Hvornår skal vi eksempelvis i ord begynde at indikere, at det er overvejende sandsynligt, at PTA vil vare ved, og at der umiddelbart er tale om en mere vedvarende tilstand, og hvad skal vi i givet fald kalde denne tilstand? (figur 11)
Figur 10 – udarbejdet af neuropsykolog Christina Engelmann
Figur 11 - udarbejdet af neuropsykolog Christina Engelmann
Vurdering/rating-scales
Grad af bevidsthedssvækkelse kan være vanskelig at vurdere, da patienten kan:
- have nedsat og svingende arousal (og awareness).
- være udtrættet (patienten kan endda være sovende).
- være motorisk svækket (eksempelvis paralyse eller spasticitet).
- have sensoriske forstyrrelser (eksempelvis blindhed, døvhed).
- have diverse kognitive forstyrrelser (eksempelvis afasi, ”apraksi”, nedsat opmærksomhed etc.).
- have epileptiforme fænomener.
- have konkurrerende sygdomme (eksempelvis hydrocephalus, infektioner).
- være påvirket af medicinering/sedering.
- Og meget andet …
Risikoen for at tage fejl i vurderingen af svær bevidsthedssvækkelse er stor (37 % ifølge Childs et al, 1993; 43 % ifølge Andrews et al, 1996; 41 % ifølge Schnakers et al, 2009), men risikoen mindskes markant ved øvede undersøgere og ved anvendelse af målrettede ratingscales (eksempelvis Løvstad et al, 2010). Der findes et svensk studie (Godbolt et al, 2011), der i høj grad yderligere understøtter den store risiko for fejldiagnosticering. Her blev der sendt spørgeskemaer ud til 3259 svenske læger med virke inden for blandt andet neurokirurgi, neurologi, geriatri og rehabilitering (1068 besvarede alle spørsgmål, svarende til ca. 33 %). Spørgsmålene var relateret til mennesker, der er svært bevidsthedssvækkede, herunder også spørgsmål om kendskab til definition af vegetativ tilstand. Kun halvdelen af de adspurgte rapporterede, at de kendte definitionen på vegetativ tilstand.
Som udgangspunkt er korrekt klinisk vurdering et detektivarbejde, som forudsætter gentagne (og tidskrævende) vurdering ved trænede undersøgere, der har et solidt kendskab til de diagnostiske kriterier for svær bevidsthedssvækkelse (fx Løvstad et al 2010; Godbolt et al 2012). Det kræver så mange informationer om patientens aktuelle adfærd og reaktionsmønstre som overhovedet muligt. Det er således vigtigt at observere patienten i så mange situationer som muligt, herunder samle informationer fra alle de mennesker, der er i kontakt med patienten (tværfagligt personale og pårørende). Det er også vigtigt at sørge for, at arousal hos patienten er så højt som muligt, herunder udelukke udtrætning, søvn, sløvende medicin, epileptiforme fænomener etc. Man kan i diagnosticeringsøjemd overveje manuelt at prøve at øge arousal hos patienten ved muskulær stimulation og/eller mobilisering.
Det skal påpeges, at der er stor risiko for falsk-negative svar både i klinikken og billeddiagnostisk. Man skal således være særligt opmærksom på, at manglende observationer om målrettet adfærd ikke nødvendigvis behøver betyde, at der ikke eksisterer et ”arbejdende sind” hos patienten. Det er blot en konstatering af, at man ikke har observeret målrettet adfærd hos patienten.
I det følgende beskrives udvalgte vurderingsredskaber til henholdsvis vurdering af bevidsthedssvækkelse og varighed af PTA.
Glasgow Coma Scale (GCS) blev oprindelig introduceret med henblik på at rate/vurdere ændringer i bevidsthedsniveau og/eller funktionsniveau hos patienter, der har været udsat for TBI, men skalaen vandt hurtigt indpas og er siden blevet anvendt til også at beskrive bevidsthedsniveau og/eller funktionsniveau hos alle andre neurologiske og neurokirurgiske patientgrupper. GCS kan anvendes til at give et øjebliksbillede af patientens bevidsthedsmæssige tilstand, ligesom man ved kontinuerlig anvendelse af GCS flere gange dagligt vil kunne få et mål for patientens bevidsthedsmæssige tilstand over tid. GCS har imidlertid en begrænset værdi ift. diagnosticering, da skalaen ikke skelner mellem refleksiv/tilfældig adfærd og meningsfulde/målrettede bevægelser (såsom visuel følgen/funktionel objektbrug), der netop indikerer overgangen fra VS/UWS og MCS. Der er også udfordringer i forhold til at vurdere intuberede patienter, og på den baggrund udviklede Wijdicks et al. i 2005 en ny skala i form af Full Outline of UnResponsiveness (FOUR). FOUR-skalaen har i modsætning til GCS mål for eksempelvis viljesbestemt blinken, men samlet set kan hverken GCS eller FOUR-skalaen anvendes som detaljerede måleinstrumenter for, om patienten er i VS/UWS eller MCS. Der er gennem tiden udviklet adskillelige ”coma-scales”: Herunder Coma Recovery Scale—Revised/CRS-R; Disorders of Consciousness Scale/DOCS; Sensory Modality and Rehabilitation Technique/SMART; Sensory Stimulation Assessment Measure/SSAM; Wessex Head Injury Matrix/WHIM; Western Neurosensory Stimulation Profile/WNSSP). ”The golden standard” for vurdering af bevidsthedsniveau hos mennesker med svær bevidsthedssvækkelse, er med tiden blevet JFK Coma Recovery Scale-R (CRS-R) (Giacino, Kalmar & Whyte, 2004), der er bygget op omkring ”Aspen-kriterierne” (http://www.archives-pmr.org/article/S0003-9993(04)00477-0/pdf). Man kan overveje at supplere CRS-R med Individualized Quantitative Behavioural Assessment (IQBA) (Dipasquale & Whyte, 1996; Whyte & Dipasquale, 1999: Whyte, 2005; Majerus et al, 2005; Giacino et al, 2005; Owen et al, 2009), når/hvis man er i tvivl om, hvorvidt patientens adfærd er målrettet eller ej. IQBA kan eksempelvis udføres ved, at man i første omgang observerer, hvilke(n) bevægelser patienten er i stand til at lave, og så dernæst føre et regnskab over, om patienten laver denne bevægelse sikkert hver gang på opfordring (viljesstyret følgen af verbal opfodring), om patienten også bevæger andre dele af kroppen på samme tid (støj), og om patienten ikke laver bevægelsen, når man ikke beder om det.
PTA kan vurderes både retrospektivt og prospektivt. Retrospektivt ved at interviewe patienten, efter han/hun er kommet ud af PTA, og prospektivt ved at interviewe/vurdere/rate patienten undervejs, mens patienten er i PTA. Der findes mange forskellige prospektive rating-scales til vurdering af varighed af PTA (eksempelvis Galveston Orientation and Amnesia Test (GOAT) ved Levin et al, 1979; The Westmead Scale ved Shores, 1989; Orientation Group Monitoring System (OGMS) ved Mysiv et al, 1990; Modificeret GOAT (AGOAT) ved Jain et al, 2000; The Orientation Log (O-LOG) ved Jackson et al, 2000; The Confusion Assessment Protocol (CAP) ved Sherer et al, 2005).
Guldstandarden til vurdering af PTA er The Galveston Orientation and Amnesia Test (GOAT) (Levin et al, 1979). GOAT er et standardiseret og valideret klinisk undersøgelsesredskab. Skalaen måler patientens orientering i tid, sted og egne data samt patientens evne til at huske eller fastholde oplysninger omkring skaden og indlæggelsen. Rating med GOAT kan først påbegyndes, når patienten er i stand til at samarbejde til (kort) samtale. Nogle patienter kan ikke kooperere fuldstændigt til GOAT eksempelvis på grund af (tale-)motoriske vanskeligheder. I de tilfælde kan man overveje alternative kommunikationsformer eksempelvis modificere ratingen ved, at patienten skriver sine svar, udpeger/staver på fortrykte, skrevne plancher, eller ved at man som undersøger omformulerer spørgsmålene til multiple-choice og/eller stiller "ja/nej”-spørgsmål. Andre patienter kan blot delvist kooperere til GOAT, hvorfor det kan være nødvendigt at ændre i standardproceduren. Man bør som udgangspunkt ændre så lidt i standardproceduren som muligt, idet hver enkelt lille ændring påvirker reliabiliteten såvel som validiteten. Hos enkelte patienter (eksempelvis hos patienter med svær afasi eller svære opmærksomhedsproblemer) er det slet ikke muligt at anvende GOAT. I sådanne tilfælde kan man overveje at foretage et mere klinisk skøn af længden af PTA, herunder indhente informationer om, hvorvidt patienten er i stand til at fastholde nye informationer fra dag til dag (gerne ud fra tværfaglige observationer – kan patienten eksempelvis finde sine ting på stuen, finde vej på afsnittet/hospitalet, genkende personale, huske aftaler, og hvornår blev patienten i stand til dette).
Der findes også adskillige rating-scales til at vurdere og potentielt prospektivt vurdere/beskrive funktionsniveauet hos den enkelte patient, herunder Glascow Outcome Scale (GOS), Glascow Outcome Scale Extended (GOSE), Disability Rating Scale (DRS), Early Functional Abilities (EFA), Functional Independence Measure (FIM), The Rancho Los Amigos Levels of Cognitive Functioning Scale (RLA) med flere.
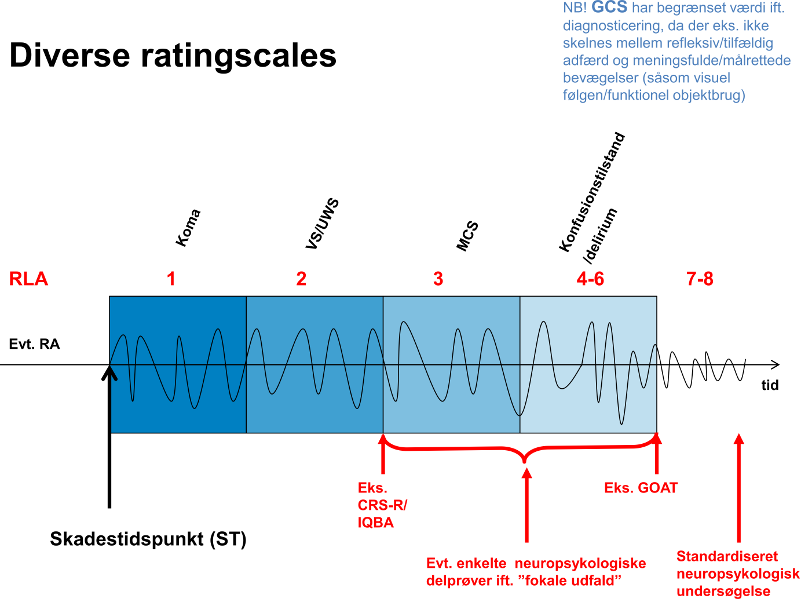
The Rancho Los Amigos Levels of Cognitive Functioning Scale (RLA) er en skala, som beskriver de mønstre eller niveauer af bedring, der typisk ses hos voksne patienter, der har været udsat for TBI med initial svær bevidsthedssvækkelse (svarende til koma, VS/UWS, MCS). Beskrivelsen involverer adfærdsmæssige karakteristika og kognitive funktioner. RLA er også kendt som The Rancho Scale eller Levels of Cognitive Functioning Scale (LCFS) - figur 12.
RLA blev udviklet af et tværfagligt team fra Rancho Los Amigos Hospital i Californien (Hagen, Malkmus & Durham, 1979; Hagen, 1984). Skalaen er baseret på observationer af bedringsforløb hos 1000 patienter, som alle havde været udsat for TBI (Malkmus, Booth & Kodimer, 1980). Den oprindelige skala har 8 niveauer, men der findes også en skala med 10 niveauer, hvor niveau 8 blev opdelt i niveau 8, 9 og 10.
RLA har vundet stor udbredelse internationalt og anvendes specielt af sundhedspersonale til at klassificere patienter og følge patientens fremskridt gennem hele bedringsprocessen. Skalaen har vist sig værdifuld for såvel det behandlende team som pårørende i form af en støtte til at forstå den enkelte patients aktuelle adfærd samt udviklingen i patientens tilstand under hele forløbet.
I den oprindelige udgave af RLA var der 8 niveauer, men i 1998 udvikledes den tredje udgave af RLA med i alt 10 niveauer (Hagen, 1998). Den tredje udgave af RLA er ikke valideret.
Figur 12 – tilpasset fra The Rancho Los Amigos Levels of Cognitive Functioning Scale (RLA) (Hagen et al, 1979, 1984 & 1998). Oversat til dansk af overlæge Aase Engberg
Som neuropsykolog bliver man ikke sjældent bedt om at vurdere/teste et menneske, der enten er bevidsthedspåvirket eller befinder sig i en form for konfusionstilstand (eksempelvis PTA). I første omgang bør man (som altid) kraftigt overveje formålet med testningen. Neuropsykologisk standardiseret testning (forstået ved anvendelse af psykometriske tests til at vurdere sandsynligheden for kognitive svigt, herunder foreneligheden med en kendt eller ikke kendt cerebral påvirkning) kan ikke sjældent lade sig gøre, men det er vigtigt at stille sig selv og andre spørgsmål om, hvad formålet med testningen er. Man skal være opmærksom på, at regelret testning ikke giver et sikkert billede af patientens aktuelle kognitive vanskeligheder og ressourcer, da patientens tilstand/præstationer ofte fluktuerer markant over et døgn i denne fase. Testning kan eventuelt give et hint om fokale udfald til hjælp i klinikken, men disse fokale udfald er der ikke nødvendigvis (i samme grad), når/hvis patienten kommer ud af konfusion, herunder PTA. Det kan til gengæld give god mening at beskrive patientens tilstand, når den er bedst og dårligst set over et døgn. Herunder i form af talværdier (eksempelvis fra førnævnte rating-scales) og resultater fra enkelte neuropsykologiske prøver med det formål at belyse eventuelle forstyrrelser, der aktuelt vil kunne give give anledning til misforståelser i omgivelserne (eksempelvis kan tegneprøver anvendes til at illustrere neglekt-fænomener) – jvf. figur 13.
Figur 13 - udarbejdet af neuropsykolog Christina Engelmann
I de senere år er man i stigende grad begyndt at inddrage billeddiagnostiske undersøgelser og/eller elektrofysiologiske teknikker i diagnosticeringen af bevidsthedssvækkede patienter (eksempelvis CT, MR, DTI, PET, MR-spectografi, fMRI, EEG, MEG og TMS) og flere af teknikkerne alene eller i kombination har vist sig brugbare som led i diagnosticering, omend ikke 100 % sikre på individ-plan (eksempelvis Voss et al, 2006; Gosseries et al, 2011; Lehembre et al, 2012; Casali et al, 2013; Napolitani et al, 2014; Guller og Giacino 2014). Ingen af de nævnte teknikker kan ej heller (endnu?) sige noget helt sikkert om outcome hos den enkelte patient, men flere af teknikkerne kan på hver sin måde bidrage til at øge forståelsen af den menneskelige bevidsthed (på gruppeplan og indimellem på individuelt plan) (eksempelvis Gosseries et al, 2014; Giacino et al, 2014). Et i dag klassisk eksperiment ved Owen et al. (2006) viste anvendeligheden af fMRI i forståelse og diagnosticering af mennesker med DOC. Owen et al. (2006) undersøgte en 23-årig kvinde, der under en trafikulykke blev udsat for en svær traumatisk hjernepåvirkning. Ud fra et klinisk skøn baseret på ”Aspen-kriterierne” havde kvinden befundet sig i VS/UWS med en rimelig fast døgnrytme efter skadestidspunktet. Når kvinden 5 måneder efter skadestidspunktet (stadig i ”klinisk VS/UWS”) og raske kontrolpersoner blev lagt i en MR-skanner og blev givet specifikke instruktioner om at forestille sig at udføre handlinger, så indicerede fMRI ens hjerneaktivitet i begge ”grupper” – (se Owen et al, 2006, figur 1, side 1402 http://orbi.ulg.be/bitstream/2268/130307/1/VS_science2006.pdf). Dette fænomen, hvor patienter i klinikken ikke udviser tegn på ”awareness”, men billeddiagnostisk eller elektrofysiologisk udviser en eller anden form for cerebral lokaliseret reaktion/rettehed/fokusering mod omgivelserne, kaldes i dag for Funktionel Locked-In (LIS*). Terminologien er foreslået af Coma Science Group, se tidligere (http://www.coma.ulg.ac.be/). Det store spørgsmål er så, om patienter i LIS* som helhed er ”aware” eller ikke-aware”, hvilket vi med vores viden i dag ikke kan svare helt klart på. Flere billeddiagnostiske studier har utvetydigt vist, at mennesker i MCS er i stand til sikkert og målrettet at reagere på smertestimuli (Boly et al, 2005, 2007; Schnakers et al, 2007, 2009), hvorfor man altid kraftigt bør overveje profylaktisk at smertebehandle mennesker i MCS.
Behandling/rehabilitering/tiltag
Der findes umiddelbart ingen medicinsk behandling, der kan øge bevidsthedsniveauet som helhed hos patienter, der er svært bevidsthedssvækkede efter TBI, men der er lavet studier, som viser en vis positiv effekt på arousal-niveauet hos nogle patienter ved brug af for eksempelvis anti-parkinson-midler eller medicin mod sklerose-træthed såsom apomorfin og specielt amantadin, ligesom et ”sovemiddel” som zolpidem hos nogle patienter har vist en paradoks-effekt og øget arousal (Chatelle et al, 2014; Giacino et al, 2012 & 2015; Whyte et al, 2013; Gosseries et al, 2014; Hammond et al, 2015). Det skal også tilføjes, at der er nogle etiske overvejelser at gøre sig i forhold til anvendelse af anti-parkinson-præparater som helhed, da L-Dopa og anden anti-parkinson medicin har vist øget risiko for forstyrrelser med impulskontrol og anden tvangsadfærd såsom ludomani, overdreven dyrkelse af en hobby, overdreven risikovillighed, tvangskøb, overspisning, hyperseksualitet med videre + dopamin-dysreguleringssyndrom (eksempelvis Callesen et al, 2013). Parkinson-foreningen har udgivet en pjece, der detaljeret gennemgår netop impulskontrolforstyrrelser (http://www.parkinson.dk/).
Flere har forsøgt med Deep-brain Stimulation/DBS for at øge ”bevidstheden” hos svært bevidsthedssvækkede patienter (eksempelvis thalamisk stimulation, Schiff et al, 2007), men der er umiddelbart få cases og flere med blandet effekt. Dertil kommer de etiske overvejelser i forhold at lave et så operativt indgreb samt igen overvejelserne omkring bivirkninger, herunder at DBS af subthalamiske kerner også er associeret med impulskontrol-forstyrrelser (Lyons, 2011).
Der er også forsøgt med rTMS (repetetiv transkraniel magnetisk stimulation), men (endnu?) uden sikker effekt (Pistoia et al, 2013).
Der findes efter mit kendskab ingen prospektive kontrollerede studier, der på nuværende tidspunkt har vist, at eksempelvis ”strukturereret sansestimulation” eller specifikke former for fysioterapeutisk, ergoterapeutisk, neuropsykologisk, logopædisk, specialpædagogisk, sygepleje (eller anden faggruppe) træning, der i sig selv kan øge bevidsthedsniveauet som helhed, men studier af tidlig mobilisering og specialisereret tværfaglig træning tyder på en vis effekt (eksempelvis Makcay et al, 1992; Seel et al, 2013; Poulsen et al, 2014).
I forhold til mobilisering er der ved ph.d.- studerende fysioterapeut Christian Riberholt igangsat et randomiseret kontrolleret forsøg involverende patienter med TBI, der allerede på en Neurointensiv Afdeling om muligt skal mobiliseres/trænes på vippebræt. Formålet med projektet er at undersøge, om en tidlig og intensiv træningsindsats har betydning for forskellige fysiologiske parametre, funktionsniveau og bevidsthedsniveau. Undersøgelserne foregår både på Neurointensiv Afdeling på Rigshospitalet/Blegdamsvej og på Afdeling for Højt Specialiseret Neurorehabilitering på Rigshospitalet/Glostrup med udefunktion på Hvidovre Hospital.
I forhold til behandling af PTA er der heller ikke nogen klare svar. Man har på Århus Universitetshospital afprøvet metoden Reality Orientation (RO) for at mindske varighed af PTA (33 i interventionsgruppe og 43 i kontrolgruppe). Ved RO orienteres (og informeres) patienten kort fortalt vedvarende både på skrift (tavle og andet) og mundtligt i tid, sted og egne data. Ud fra dette danske studie fandt man umiddelbart ikke nogen sammenhæng mellem varighed af PTA og RO, men man fandt dog en sammenhæng mellem RO og score på Glasgow Outcome Scale Extended (GOS-E) 12 måneder efter skadestidspunkt (Langhorn et al, 2014). Tidligere havde De Guise et al 2005 i et pilotprojekt med 12 patienter udsat for TBI imidlertid fundet en sammenhæng mellem PTA og RO, hvor PTA-varighed blev reduceret med 5 dage efter vedvarende RO (resultater dog ikke statistisk signifikante). RO er også afprøvet på andre patientgrupper med god effekt, eksempelvis på mennesker med demens (Spector et al, 2003).
I forhold til behandling af delirium er der på vegne af ph.d.-studerende sygeplejerske Laura Krone Larsen på Neurointensiv Afdeling på Rigshospitalet/Blegdamsvej igangsat en klinisk kontrolleret undersøgelse af delirium før og efter implementering af en systematisk interventionspakke (indeholdende blandt andet optimering af sedationspraksis, smertevurdering, mobilisering og søvn/hvile under indlæggelse på Neurointensiv Afdeling). Projektet hedder "DANDELION. Dansk deliriumundersøgelse af neurointensive patienter", og yderligere information om projektet kan fås på https://clinicaltrials.gov/ eller ved henvendelse til projektsansvarlig laura.krone.larsen@regionh.dk.
Som allerede nævnt under afsnittet om begrebsafklaring, så findes der ingen specifik behandling for agitation, men noget tyder på, at kognitiv bedring mindsker risikoen for agitation (Bockbrader, 2015), ligesom behandling af konkurrerende sygdomme kan mindske risikoen for agitation, herunder også fokus på at genvinde døgnrytme og mindske irrelevante stimuli (Bogner et al, 2015). Man kan derfor overveje medicinsk støtte til at opretholde en rimelig døgnrytme (det kan være ”sovemedicin”, men også melatonin kan være en mulighed).
På nuværende tidspunkt tyder det ikke på, at man kan forcere bedringsprocessen (”trykke på knapper”) hos patienter med TBI. Man kan ved nogle former for behandling (se ovenfor) måske øge arousal hos nogle få patienter, og måske finde medicinsk årsag eller anden kilde til agitation og derved afhjælpe dette. Man kan endvidere mindske de ”sekundære skader” (se ovenfor) og således understøtte en proces, som forhåbentlig er i gang hos patienten, ligesom man kan fokusere på at tilpasse træningen til patientens bevidsthedsniveau. Ved sidstnævnte menes der, at man kan forsøge at fokusere endnu mere på den ”kompenserende indsats” – nedenstående forslag i boks 1-4 ved neuropsykolog Christina Engelmann er ikke en facit-liste, men skal nærmere betragtes som inspiration i tilgangen til patienten.
Boks 1 – udarbejdet af neuropsykolog Christina Engelmann
| Kompenserende indsats for den svært bevidsthedssvækkede patient |
|
|---|
Boks 2 – udarbejdet af neuropsykolog Christina Engelmann
| Kompenserende indsats for den konfuse patient (skærm og korriger… så vidt muligt) |
|
|---|
Boks 3 – udarbejdet af neuropsykolog Christina Engelmann
| Hovedpunkter i forhold til den konfuse patient |
|
|---|
Boks 4 – udarbejdet af neuropsykolog Christina Engelmann
| Endnu mere konkrete tiltag (men vær igen opmærksom på, at det er taget ud af en sammenhæng, og at der ikke er en sandhed, som kan trækkes ned over alle mennesker) |
|
|---|
Bevidsthedssvækkelse og det neurale grundlag
Eksperimentelle studier hos raske mennesker tyder på, at ”bevidst hjerneaktivitet” typisk er associeret med adskillelige hjerneregioner i både præfrontale og parietale cortex (eksempelvis Dehaene et al, 2003, 2006, 2011). Det samme billede gør sig gældende i undersøgelser af patienter, der er eller har været svært bevidsthedssvækkede grundet TBI (Laureys et al, 1999 og 2005; Giacino et al, 2015). Det vil sige, at alt tyder på, at bevidsthed ikke er placeret et enkelt sted i hjernen, men nærmere involverer flere områder/regioner og neurale netværk i hjernen. I det følgende vil en lille del af de utallige undersøgelser, der er lavet omkring bevidsthedssvækkelse og det neurale grundlag, blive gennemgået.
Nogle har stillet spørgsmål ved om den globale cerebrale metabolisme (hele hjernens stofskifte) kan fortælle noget om grad af bevidsthedssvækkelse, men det har hidtil vist sig, at det globale stofskifte i hjernen ikke nødvendigvis stiger, når ”bevidsthedsniveauet” stiger (ingen markant ændring fra VS/UWS til MCS) (se Laureys et al, 2004, figur 4, side 540 http://www.coma.ulg.ac.be/papers/vs/PVS_MCS_LIS_LancetN04.pdf). Et nyligt FDG-PET studie med dansk islæt (samt bl.a. Laureys og Thibaut) udfordrer imidlertid Laureys et al, 2004 ved at vise en sammenhæng mellem den globale cerebrale glucose-metabolisme og bevidsthedsniveau.
Hos 131 patienter med DOC (28 raske kontroller i hvile) fandt man nemlig nogle ret stabile grænser mellem de forskellige bevidsthedstilstande (for patienter i VS/UWS var hjerneaktiviteten 38 procent af normalen, for patienter i MCS var hjerneaktiviteten 56 procent af normalen, for patienter som var kommet ud af MCS var hjerneaktiviteten på 63 procent af normalen). På denne baggrund beregnedes ”cut-off-score” i den forstand, at 40-45 procent af normal hjerneaktivitet skønnedes at være en ret klar skillelinje mellem VS/UWS og MCS, omend ikke en 100 % sikker skillelinje (Stender et al, 2016).
Hvis ikke den globale metabolisme kan give nogle helt sikre svar, kan den regionale metabolisme så? Det viser sig faktisk, at der hos nogle mennesker med svær bevidsthedssvækkelse findes eksempler på isolerede neurale netværk (regionalt øget/normal metabolisme i PET-studier), herunder antydning af øer med bevaret funktion (eksempelvis at patienter kan tale eller gå uden at udvise anden form for isoleret rettethed af opmærksomhed mod sig selv eller omgivelserne). Følgende eksempler på ”isolerede neurale netværk” antyder, at det er muligt at have fungerende isolerede subnetværk af funktion uafhængigt at, om patienten selv er opmærksom på eller bevidst om dette (eller at ”bevidste områder/netværk af hjernen får besked herom):
- De Jong et al, 1997, beskrev en patient i klinisk VS/UW, som ved PET-studie viste øget metabolisme specifikt i gyrus cingularis anterior og i temporale regioner, når patienten blev præsenteret for auditive stimuli i form af historie-oplæsning fra sin mor. Patienten viste ikke samme cerebrale aktivitet, når det var oplæsning fra ikke-velkendte stemmer. Hos raske kontrolpersoner sås aktivitet i de samme områder, når de lyttede til for dem velkendte stemmer.
- Menon et al, 1998, beskrev en patient i klinisk VS/UWS, som ved PET-studie viste øget metabolisme i ”visuelle associationsområder” (eksempelvis gyrus fusiformis i højre hemisfære), når patienten blev præsenteret for familiære/velkendte ansigter i modsætning til ingen specifik aktivitet i selv samme område, når patienten blev præsenteret for ”meningsløse visuelle billeder”. Det skal hertil tilføjes, at det er velkendt, at metabolismen øges specifikt i gyrus fusiformis i højre side hos raske kontrolpersoner, når de præsenteres for familiære/velkendte ansigter (Haxby et al, 1994, 2000).
- Schiff et al, 1999, beskrev en kvinde, der efter TBI havde været i klinisk VS/UWS i 20 år. Kvinden producerede somme tider enkle forståelige ord uden stimuli fra omgivelserne, men opfyldte ellers kriterier for VS/UWS (verbaliseringerne skete sjældent, og det er ikke registreret, hvornår de begyndte). Ved nærmere undersøgelser viste den global cerebrale metabolisme sig at være på omtrent 55 % i forhold til det forventede niveau. PET viste regionale ”øer” af højere metabolisme i venstre pars opercularis og pars triangularis (”Brocas område”), venstre temporo-parietale områder samt anteriore del af basalganglierne. Samlet tyder dette case-studie på isolerede ”neurale øer”, der giver fragmenter af aktivitet hos en VS/UWS-patient med en svært skadet hjerne. Hypotesen er, at det er isolerede thalamus-kortikale-basalganglie-loops, der ligger til grund for kvindens adfærd.
- Laureys et al, 2002, undersøgte 15 patienter i klinisk VS/UWS (ætiologi?), der blev PET-skannet og samtidig smertepåvirket (non-invasiv elektrisk stimulation). Ved smertepåvirkning sås alene aktivering af mellemhjerne, thalamus og primære sensoriske områder (kontralateralt), men ingen aktivering af sekundære sensoriske områder, insula, posteriort parietalt eller i gyrus cingularis anteriort, som der derimod sås hos raske kontrolpersoner. Ud fra dette formuleredes en hypotese om isolerede neurale netværk hos nogle patienter i VS/UWS.
Ud fra ovenstående studier, så tyder det altså på, at den regionale metabolisme spiller en rolle, men undersøgelserne giver ikke svar på, om det er bestemte strukturer/områder i hjernen, der skaber awareness/rettethed af opmærksomhed/”bevidsthed”, om det er neurale netværk, eller om det er begge dele.
Et ad de meste velbeskrevne single-case-studier af late-recovery af Voss et al, 2006, indikerer, at hvid substans (grundbestanddel i de neurale netværk) spiller en central rolle i processering af bevidsthed. Det drejer sig om den ved studiets begyndelse 40-årige mand (Terry Wallis), der 19 år tidligere havde været udsat for svær TBI efter en bilulykke. Patienten havde klinisk været MCS i de sidste 19 år, hvorefter han pludseligt udviste spontan bedring. Patienten var svært paretisk og havde svære kontrakturer, men kunne pludseligt tale spontant (med svært dysartrisk tale) og kunne forstå tale. Der skete betydelig bedring i funktionsniveauet i de to år, hvor patienten blev fulgt intensivt blandt andet i hverdagssammenhænge og billeddiagnostisk. Der sås uændret nedsat global metabolisme sammenlignet med raske kontrolpersoner - også efter to års funktionel bedring. MR viste uændret omfattende atrofi kortikalt og subkortikalt (specielt i hjernestammen og frontallapperne samt udvidede ventrikler) og svær diffus aksonal skade (DAI) (eksempelvis var corpus callosum kun 1/3 til 2/3 af størrelsen hos raske kontrolpersoner). I de første to år, hvor patienten blev fulgt, steg mængden af hvid substans i specielt posteriore kortikale områder og i cerebellum. Den samlede hypotese lød, at ved late-recovery tyder det på, at en langsom strukturel ændring (eksempelvis i mængden af hvid substans) i hjernen kan hænge sammen med bedring.
Hvis det nu viser sig, at regenerering af hvid substans er essentiel for genvindelse af awareness, hvor meget skal der så til, og er der en tærskelværdi? Derudover er det så specifikke strukturer/områder i hjernen eller specifikke netværk mellem specifikke strukturer, der spiller en særlig rolle?
- Et studie omhandlende regional cerebral metabolisme indikerer, at præcuneus (område i mediale parietale cortex) og posteriore del af gyrus cingularis/cingulate cortex (grænsende op til præcuneus) også spiller en rolle i processering af bevidsthed. Laureys et al, 2004, undersøgte mennesker i forskellige bevidsthedstilstande og fandt, at præcuneus og posteriore del af gyrus cingularis/cingulate cortex var det område, der er mest aktivt hos raske kontrolpersoner i hviletilstand (ikke under søvn), hvorimod det er det område, som er mindst aktivt hos patienter i VS/UWS (se Laureys et al, 2004, figur 7, side 543, http://www.coma.ulg.ac.be/papers/vs/PVS_MCS_LIS_LancetN04.pdf). Det tyder på, at præcuneus også er det område, der er mindst aktivt under dyb søvn og ved generel anæstesi (Vogt et al, 2005). Dog ses ved anæstesi-induceret bevidsthedssvækkelse en specifik regional reduktion af aktivitet i thalamus (Alkire 2009), men det er uafklaret, om der er reduktion et andet sted før reduktion i thalamus.
- Laureys et al, 2000, beskrev en 28-årig mand, der havde været i klinisk VS/UWS i 2 måneder efter hjertestop grundet heroin-overdosis. Patienten udviste spontan bedring efter 2 måneder – først MCS, siden konfusion og senere delvist selvhjulpen (uvist om og hvornår han skønnedes ude af konfusionstilstand). Patienten blev fulgt med MR og FDG-PET, som viste en ændring i forbindelserne mellem de intralaminære thalamiske nuclei og præfrontale områder (inklusiv anteriore cingulate cortex), og at disse forbindelser genetableredes, da patienten genvandt awareness.
- Schiff et al, 2007, beskrev i et single-case-study, at Deep Brain Stimulation (DBS) af netop de intralaminære nuclei i thalamus formentlig medførte konsistent målrettet adfærd hos en patient, der havde været i MCS efter TBI i 6 år op til dette – patienten kunne kort tid efter DBS eksempelvis som noget nyt indtage mad oralt.
Hvis man ser på de neurale netværks rolle i forhold til processering af bevidsthed, så viste Laureys et al allerede i 1999, at både specifikke strukturer/områder netværk spiller en rolle. Eksempelvis beskrev Laureys et al, 1999, en 40-årig kvinde, der efter selvmordsforsøg (kulilteforgiftning) var i klinisk VS/UWS i 19 dage og pludselig udviste bedring, således at hun havde genvundet en sammenhængende hukommelse for begivenheder fra dag til dag efter 4 uger. I denne periode sås ved FDG-PET øget metabolisme i parietale og præfrontale områder. Et år efter selvmordsforsøget beskrives lettere kognitive problemer, hvilket var en forværring sammenlignet med skøn fra før selvmordsforsøget, men en markant bedring over tid.
Som tidligere antydet, så er det ikke alene patienter i VS/UWS, der udviser ændringer i bevidsthedsniveau, herunder forskelle mellem arousal og awareness. Mennesker med epilepsi i form af abscence-anfald eller komplekse partielle anfald (dette begreb er bortfaldet i de nyeste klassifikationer fra ILAE - Internationale sammenslutning af fagpersoner som arbejder med epilepsi) samt søvngængeri (en enkelt case) udviser også (om end forbigående) bevaret arousal, men (midlertidige) ændringer i awareness (se Laureys, 2005, Figur 1 i Box 1, http://orbi.ulg.ac.be/bitstream/2268/2393/1/Laureys%20trends%20cogn%20scie2005.pdf
–NB! Ifølge det nyeste klassifikationssystem fra (International League Against Epilepsy (ILAE) i 2017, da betegnes complex partiel seizure nu som focal impaired awareness, ligesom absence seizure nu betegnes som generalized non-motor seizure.
Samlet set så udviser patienter I klinisk VS/UWS cerebral aktivitet begrænset til subkortikale og (primært) kortikale områder, men disse områder er afbrudt i forbindelsen til det fronto-parietale netværk, som er nødvendigt for awareness (Laureys, 2005; Giacino et al, 2006 & 2015; Giacino & Schiff, 2009), hvorfor man betragter svær bevidsthedssvækkelse som ”a disconnection syndrome” mellem kortikokortikale netværk (prefronto-parietale netværk) og/eller kortiko-thalamiske(eventuelt også striatale)-kortikale netværk. Nyere studier tyder endda på endnu større kompleksitet, herunder også ”disconnection” eller afbrydelse af auditive, visuelle og/eller sensoriske netværk (Demertzi et al, 2015).
Bevidsthed og teoretiske konstruktioner
Der er gennem tiden udviklet flere og flere teoretiske modeller/konstruktioner til at beskrive (aspekter af) den cerebrale processering af bevidsthed, herunder eksempelvis:
- Default Mode Network (DMN) (beskrevet gradvist først som ”Stream of consciousness” af William James i 1890; af Hans Berger i 1931 som var ”Grundlægger” af EEG - fandt EEG-mønstre, når mennesker slappede af (Stone et al, 2013); af Schulman et al i 1997, som ved PET-studier beskrev en deaktiveringstilstand; af Raichle et al i 2001, som samlede beskrivelserne om DMN og introducerede begrebet Default Mode; af Buckner et al 2008, som introducerede begrebet Default Mode Network (DMN). Nogle studier har vist, at DMN ikke umiddelbart er aktivt hos patienter der opfylder hjernedødskriterierne (Boly et al, 2009), men at DMN derimod er delvist bevaret hos patienter i VS (Cauda et al, 2009; Vanhaudenhuyse et al, 2010; Soddu et al, 2012)
- Salience Network (SN) (Menon, 2015; Beissner, Meissner, Bar, & Napadow, 2013; Lovero, Simmons, Aron, & Paulus, 2009; Menon & Uddin, 2010; Seeley et al., 2007; Sridharan et al., 2008)
- The Mesucircuit Model (Giacino et al, 2014).
- The Global Workspace Theory (Baars, 1988, 1997 & 2002; Dehaene et al 2003, 2006, 2011).
Det neurale grundlag for svær bevidsthedssvækkelse nu ud fra et neuropsykologisk perspektiv
Hvad er tærskelværdien for, at noget bliver bevidst, at det kommer ind i vores opmærksomhedsfelt, at det lyser op ud af utallige indtryk? Hvad kræver det for eksempel at se en opstrakt hånd hos en deltager, mens man underviser?
- Refleksiv opmærksomhed
(det vil sige en automatiseret, forholdsvis energisparende radar, der lokaliserer ændringer i omgivelserne såsom hurtige bevægelser, høje lyde).
- Voluntær opmærksomhed
(det vil sige et prioriteringssystem, der må betragtes som en relativ energikrævende del af vores sparsomme opmærksomhedskapacitet. Et system, som står for hurtig vurdering af, om det er relevante bevægelser eller ej, herunder om der skal reageres på dem eller ej – eksempelvis at se en hånd, der bevæger sig hos deltager i undervisningen og foretage en hurtig vurdering undervejs: '”nej, det var bare en kløen i næsen”, ”ja, men jeg skal lige tale færdig”, ”ja, nu”') – jævnfør Dehaene, 2011; Chica & Bartolomeo, 2012. Så igen, hvad kræver det at følge med i opstrakte hænder, mens man samtidig bruger energi på at huske sit undervisningsmateriale samt at have en eller anden form for kontakt med sig selv og deltagerne? Det kræver:
- Et vist energiniveau (formentligt specielt hjernestamme -> thalamus (striatum)).
- En virksom radar (formentligt specielt parietal + andre ”primære sensoriske områder” <-> thalamus).
- En virksom evne til at prioritere, sortere skidt fra kanel (formentligt specielt følgende netværk: thalamus <-> præfrontal cortex/Salience Network? <-> Parietal <-> thalamus).
Hos mennesker, som er svært bevidsthedssvækkede, der er disse opmærksomhedssystem(er) afbrudte enten fuldstændigt eller delvist. Hos nogle mennesker med svær bevidsthedssvækkelse ser vi formentlig adfærd baseret på regionale øer af netværk/virksomhed, men altså ikke nok ”interconnectivity” eller gensidig forbundenhed til at nå over tærsklen til at opnå awareness.
Kilder
Ahmed S et al. Post-traumatic amnesia after closed head injury: a review of the literature and some suggestions for further research. Brain Injury 2000;14(9):765-80.
Alkire MT et al. General Anaesthesia and Consciousness I: Laureys S et al (red.), The Neurology of Consciousness – Cognitive Neuroscience and Neuropathology (2. udgave), 118-34. Academic Press, 2008.
American Academy of Neurology Guideline Process Manual. AAN.com [online], https://www.aan.com/Guidelines/Home/Development (2011).
Andrews K, Murphy L, Munday R, Littlewood C. Misdiagnosis of the vegetative state: retrospective study in a rehabilitation unit. BMJ 1996;313(7048):13–16.
Ansell BJ, Keenan JE. The Western Neuro Sensory Stimulation Profile: a tool for assessing slow to recover head-injured patients. Arch Phys Med Rehabil 1989;70:104–8.
Asikainen I, Kaste M et al. Predicting late outcome for patients with traumatic brain injury referred to a rehabilitation programme: A study of 508 Finnish patients 5 years or more after injury. Brain Injury 1998;12:95-107.
Baars Bernard J. A Cognitive Theory of Consciousness. Cambridge, MA: Cambridge University Press, 1988.
Baars Bernard J. In the Theater of Consciousness. New York, NY: Oxford University Press, 1997.
Baars Bernard J. The conscious access hypothesis: Origins and recent evidence. Trends in Cognitive Sciences 2002;6 (1):47-52.
Beissner F et al. The Autonomic Brain: An Activation Likelihood Estimation Meta-Analysis for Central Processing of Autonomic Function. The Journal of Neuroscience 2013:33(25):10503–11.
Bishara et al. Post traumatic amnesia and Glasgow Coma Scale related to outcome in survivors in a consecutive series of patients with severe closed-head injury. Brain Injury 1992;6(4):373-80.
Bockbrader MA, Mortimer D, Worthen-Chaudhari L, Rosenthal J, Corrigan J, Mysiw WJ, Bogner JA. Agitation duration, density and intensity predict rehabilitation length of stay and motor functional independence measures (FIMs) in traumatic brain injury. Arch Physical Med Rehabil 2015;95(10):E66.
Bode RK et al. Measurement properties of the Galeveston Orientation and Amensia Test (GOAT) and improvement patterns during inpatient rehabilitation. J Head Trauma Rehabil 2000;15(1):637-55.
Bogner JA et al. Predictors of Agitated Behavior During Inpatient Rehabilitation for Traumatic Brain Injury. Arch Physi Med Rehabil 2015;96(8 Suppl 3):274-81.
Boly M et al. Cerebral processing of auditory and noxious stimuli in severely brain injured patients: differences between VS and MCS. Neuropsychol Rehabil 2005;15:283-9.
Boly M et al. Perception of pain in the minimally consciuos statewith PET activation: an observational study. Lancet Neurol 2008;7:1013-20.
Boly M et al. Functional connectivity in the default network during resting state is preserved in a vegetative but not in a brain dead patient. Hum Brain Mapp 2009;30:2393-2400.
Brooke MM, Questad KA et al. Agitation and restlessness after closed head injury: A prospective study of 100 censecutive admissions. Arch Physical Med Rehabil 1992;73:320-3.
Brown AW, Malec JF, McClelland RL, Diehl NN, Englander J, Cifu DX. Clinical Elements that Predict Outcome after Traumatic Brain Injury: A Prospective Multicenter Recursive Partitioning (Decision-Tree) Analysis. Journal of Neurotrauma, 2005; 22(1):1040-51.
Buckner RL et al. The brain's default network: anatomy, function, and relevance to disease. Ann N Y Acad Sci 2008;1124:1-38.
Callesen et al, 2013. A Systematic Review of Impulse Control Disorders in Parkinson’s Disease. Journal of Parkinson’s Disease 2013;3:105–138.
Casali AG et al. A Theoretically Based Index of Consciousness Independent of Sensory Processing and Behavior. Science Translational Medicine 2013;5(198):198-205.
Cauda F et al. Disrupted intrinsic functional connectivity in the vegetative state. J Neurol Neursurg Pscychiatry 2009;80:429-31.
Chatelle C et al. Changes in cerebral metabolism in patients with a minimally conscious state responding to zolpidem. Front Hum Neurosci 2014;8:917.
Childs NL, Mercer WN, Childs HW. Accuracy of diagnosis of persistent vegetative state. Neurology 1993;43(8):1465–7.
Corrigan JD. Development of a scale for assessment of agitation following traumatic brain injury. J Clin Exp Neuropsych 1989;11(2):261-77.
Corrigan JD, Mysiw WJ et al. Agitation, cognition and attention during post-traumatic amnesia. Brain injury 1992; 6:155-60.
David AS, Fleminger S, Kopelman MD, Lovestone S, Mellers JDC. Lishman’s Organic Psychiatry – A textbook of neuropsychiatry. (4. udgave). West Sussex, UK: Wiley-Blackwell, 2009.
De Guise E et al. Effects of an integrated reality orientation programme in acute care on post-traumatic amnesia in patients with traumatic brain injury. Brain Injury 2005; 19(4):263-9.
Dehaene S, Sergent C, Changeux JP. A neuronal network model linking subjective reports and objective physiological data during conscious perception. Proc Natl Acad Sci USA 2003;100:8520-5.
Dehaene S et al. Conscious, preconscious, and subliminal processing: a testable taxonomy. Trends in Cognitive Sciences 2006;10:204-11.
Dehaene S, Changeux JP. Experimental and theoretical approaches to conscious processing. Neuron 2011;70:200–27.
De Jong BM et al. Regional cerebral blood flow changes related to affective speech presentation in persistent vegetative state. Clin Neurol Neurosurg 1997;99(3):213-6.
Demertzi A, Soddu A, Laureys S. Consciousness supporting networks. Curr Opin Neurobiol 2013;23:239–244.
Demertzi A et al. Intrinsic functional connectivity differentiates minimally conscious from unresponsive patients. Brain 2015;138:2619-31.
DiPasquale MC, Whyte J. The use of quantitative data in treatment planning for minimally conscious patients. J Head Trauma Rehabil 1996;11:9–17.
Ellenberg JH et al. Post-traumatic Amnesia as a Predictor of Outcome after Severe Closed Head Injury. Archives of Neurology, 1996;53:782-91.
Engberg AW et al. Centralized rehabilitation after severe traumatic brain injury – a population-based study. Acta Neurol Scand 2006;113:178-84.
Flemminger S. Head Injury. I: David AS, Fleminger S, Kopelman MD, Lovestone S, Mellers JDC. Lishman’s Organic Psychiatry – A textbook of neuropsychiatry. (4. udgave). West Sussex, UK: Wiley-Blackwell, 2009.
Forrester G et al. Measuring post-traumatic amnesia (PTA): an historical review. Brain Injury 1994;8(2):175-84.
Gads Psykologileksikon. (red.) Bjerg J (3. udgave). København: Gads Forlag, 2010
Giacino JT, Ashwal SA, Childs N, Cranford R, Jennett B, Katz DI, Kelly JP, Rosenberg JH, Whyte J, Zafonte RD, Zasler ND. The minimally conscious state – definition and diagnostic criteria. Neurology 2002;58:349-53.
Giacino JT, Kalmar K, Whyte J. The JFK Coma Recovery Scale-Revised: measurement characteristics and diagnostic utility. Arch Phys Med Rehabil 2004;85(12):2020–9.
Giacino, JT, Trott CT. Rehabilitative management of patients with disorders of consciousness: grand rounds. J. Head Trauma Rehabil 2004;19:254–65.
Giacino JT. Rehabilitation of Patients with Disorders of Consciousness. I: High W et al (red.), Rehabilitation for Traumatic Brain Injury, 305–37. New York: Oxford University Press, 2005.
Giacino, JT, Kalmar K. Diagnostic and prognostic guidelines for the vegetative and minimally conscious states. Neuropsychol Rehabil 2005;15:166–74.
Giacino JT, Whyte J. The Vegetative and Minimally Consciuos States - Current knowledge and Remaining Questions. J Head Trauma Rehabilit 2005;20:1:30-50.
Giacino JT, Hirsch J, Schiff N, Laureys S. Functional Neuroimaging Applications for Assessment and Rehabilitaion Planning in Patients With Disorders of Consciousness. Arch Phys Med Rehabil 2006;87(2):67-76.
Giacino JT, Schnakers C, Rodriguez-Moreno D, Kalmar K, Schiff N, Hirsch J. Behavioral assessment in patients with disorders of consciousness: gold standard or fool's gold? Prog Brain Res 2009;177:33–48.
Giacino J, Fins JJ, Machado A, Schiff ND. Central thalamic deep brain stimulation to promote recovery from chronic posttraumatic minimally conscious state: challenges and opportunities. Neuromodulation 2012;15:339–49.
Giacino JT et al. Placebo-controlled trial of amantadine for severe traumatic brain injury. N Engl J Med 2012;366(9):819-26.
Giacino JT et al. Neurorehabilitation in Disorders of Consciousness. Semin Neurol 2013;33(2):142-156.
Giacino JT et al. Disorders of consciousness after acquired brain injury: the state of the science. Nat Rev Neurol 2014;10(2):99-114.
Gill-Thwaites H, Munday R. The Sensory Modality Assessment Rehabilitation Technique (SMART): a valid and reliable assessment for the vegetative and minimally conscious state patient. Brain Injury 2004; 18:1255–69.
Godbolt et al. Opportunity for Inpatient Brain Injury Rehabilitation for Persons in a Vegetative State - Survey of Swedish Physicians. Am J Phys Med Rehabil 2011;90:482Y489.
Godbolt AK et al. Disorders of consciousness: Preliminary data supports added value of extended behavioral assessment. Brain Injury 2012;26(2):188-93.
Gosseries et al. Automated EEG entropy measurements in coma, vegetative state/unresponsive wakefulnes syndrome and minimally conscious state. Funct Neurol 2011;26:25-30.
Gosseries O et al. Disorders of consciousness: what’s in a name? NeuroRehabilitation 2011;28:3–14.
Gosseries O et al. Measuring Consciousness in Severely Damaged Brains. Annu Rev Neurosci 2014;37:457-78.
Gosseries O et al. Amantadine, apomorphine and zolpidem in the treatment of disorders of consciousness. Curr Pharm Des 2014;20(26):4146-84.
Graham DI. Pathophysiological Aspects of Injury and Mechanisms of Recovery. I: Rosenthal A (red.), Rehabilitation of the Adult and Child with Traumatic Brain Injury (3. udgave), 19-41. Philadelphia: F.A. Davies Company, 1999.
Greenwood R. Head injury for neurologists. J Neurol Neurosurg Psychiatry 2002;73(suppl 1):i8-i16.
Grosswasser Z. Medical Problems in the Management of Traumatic Brain Injury. I: Levn HS et al (Red.), Catastrophic Brain Injury, 77-92. New York: Oxford University Press, 1996.
Guller Y, Giacino JT. Potential applications of concurrent transcranial magnetic stimulation and functional magnetic resonance imaging in acquired brain injury and disorders of consciousness. Brain Injury 2014;28(9):1190–6.
Hagen C, Malkmus D, Durham P. Levels of cognitive functioning. Rehabilitation of the head injured adult: Comprehensive physical management. Dowey, CA: Professional Staff Association of The Rancho Los Amigos Hospital, Inc., 1979.
Hagen C. Language disorders in head trauma. I Holland, AL (ed.) Language disorders in adults. San Diego College Hill Press, s.245-81, 1984.
Hagen C. Levels of cognitive functioning. Rehabilitation of the head injured adult: Comprehensive physical management, third edition. Dowey, CA: Professional Staff Association of The Rancho Los Amigos Hospital, Inc., 1998.
Hammond FM et al. Psychotropic Medication Use During Inpatient Rehabilitation for Traumatic Brain Injury. Arch Phys Med Rehab 2015;96:256-63.
Haxby JV et al. The Functional Organization of Human Extrastriate Cortex: A PET-rCBF Study of Selective Attention to Faces and Locations. The Journal of Neuroscience, 1994;74(11):6X36-53.
Haxby JV et al. The distributed human neural system for face perception. Trends Cogn Sci 2000;4(6):223-33.
WHO ICD-10, Psykiske lidelser og adfærdsmæssige forstyrrelser – Klassifikation og diagnostiske kriterier. København: Munksgaard Danmark, 2006.
Jackson WT, Novack TA, Dowler RN. Effective serial measurement of cognitive orientation in rehabilitation: The Orientation Log. Arch Phys Med Rehab 1998;79:718-20.
Jain N, Layton BS, Murray PK. Are aphasic patients who fail the GOAT in PTA? A modified Galveston Orientaion and Amnesia Test for persons with aphasia. The Cinical Neuropsychologist 2000;14:13-7.
Jennett B, Teasdale G. Management of Head Injuries. Philadelphia: Davis, 1982.
Jox RJ, Bernat JL, Laureys S, Racine E. Disorders of consciousness: responding to requests for novel diagnostic and therapeutic interventions. Lancet Neurol 2012;11:732–8.
Katz D, Alexander M. Traumatic brain injury: Predicting course of recovery and outcome for patients admitted to rehabilitation. Arch Neurol 1994;51:661-70.
Klinisk ordbog (16. udgave). København: Munksgaard Danmark, 2005.
Kraus JF et al. Incidence and Prevalence of, and Costs Associated with Traumatic Brain Injury. I: Rosenthal A (red.), Rehabilitation of the Adult and Child with Traumatic Brain Injury (3. udgave), 3-18. Philadelphia: F.A. Davies Company, 1999.
Langhorn et al. Testing a Reality Orientation Program in Patients With Traumatic Brain Injury in a Neurointensive Care Unit. Journal of Neuroscience Nursing. 2014;47(1):E2-9.
Laureys S et al. Impaired effective cortical connectivity in vegetative state. Neuroimage 1999;9:377–382. http://www.coma.ulg.ac.be/
Laureys S, Lemaire C, Maquet P, Phillips C, Franck G. Cerebral metabolism during vegetative state and after recovery to consciousness. J Neurol Neurosurg Psychiatry 1999;67(1):121.
Laureys S et al. Restoration of thalamocortical connectivity after recovery from persistent vegetative state. Lancet 2000;355(9217):1790-1.
Laureys S et al. Cortical processing of noxious somatosensory stimuli in the persistent vegetative state. Neuroimage 2002;17:732–41.
Laureys S et al. Brain function in coma, vegetative state, and related disorders. Lancet Neurology 2004;3:537-46. Se www.coma-science.com
Laureys S et al. The locked-in syndrome: what is it like to be conscious but paralyzed and voiceless? Prog Brain Res 2005;150:495–511.
Laureys S. The neural correlate of (un)awareness: lessons from the vegetative state. Trends in neuroscience 2005;9(12):556-559.
Laureys S. Eyes open, Brain Shu - New brain-imaging techniques are giving researchers a better understanding of patients in the vegetative state. Scientific American 2007;maj:32-7.
Laureys S et al. Unresponsive wakefulness syndrome: a new name for the vegetative state or apallic syndrome. BMC Med 2010;8:68.
Lehembre R et al. Resting-state EEG study of comatose patients: a connectivity and frequency analysis to find differences between vegetative and minimally conscious state. Funct Neurol 2012;27:41-7.
Levin HS, O’Donnell VM, Grossman RG. The Galveston Orientation and Amnesia Test: A practical scale to assess cognition after head injury. J Nerv Ment Dis 1979;167:675-84.
Liebach A et al. Tidlig intensiv rehabilitering efter meget svær traumatisk hjerneskade – opfølgning seks måneder efter udskrivelsen. Ugeskrift for læger 2007;169(3):223-7.
Lovero KL et al. Anterior insular cortex anticipates impending stimulus significance. Neuroimage 2009;45(3):976-83.
Lyons MK. Deep Brain Stimulation: Current and Future Clinical Applications. Mayo Clin Proc. July 2011;86(7):662-72. www.mayoclinicproceedings.com
Løvstad M et al. Reliability and diagnostic characteristics of the JFK Coma Recovery Scale-Revised: Exploring the influence of rater’s level of experience. J Head Trauma Rehabil 2010;Vol. 25,No. 5:349–56.
Mackay LE, Bernstein BA, Chapman PE, Morgan AS, Milazzo LS. Early intervention in severe head injury: long-term benefits of a formalized program. Arch Phys Med Rehabil 1992;73:635–41.
Majerus S, Gill-Thwaites H, Andrews K, Laureys S. Behavioral evaluation of consciousness in severe brain damage. Prog Brain Res 2005;150:397–413.
Malkmus D, Booth B, Kodimer C. Rehabilitation of the head injured adult: Comprehansive cognitive management. Dowey, CA: Professional Staff Association of The Rancho Los Amigos Hospital, Inc., 1980.
Mckinley WW et al. Cognitive and Behavioral Effects of Brain Injry. I: Rosenthal A (red.), Rehabilitation of the Adult and Child with Traumatic Brain Injury (3. udgave), 3-18. Philadelphia: F.A. Davies Company, 1999.
Medical aspects of the persistent vegetative state (1). The Multi-Society Task Force on PVS. N Engl J Med 1994;330:1499–508.
Medical aspects of the persistent vegetative state (2). The Multi-Society Task Force on PVS. N Engl J Med 1994;330:1572–9.
Menon V et al. Cortical processing in persistent vegetative state. Lancet 1998;352:200.
Menon V, Uddin LG. Saliency, switching, attention and control: a network model of insula function. Brain Struct Funct 2010;241(5-6):655-67.
Menon V. Salience Network. In: Arthur W. Toga, editor. Brain Mapping: An Encyclopedic Reference. Academic Press: Elsevier. 2015;2:597-611.
Mysiv WJ, Corrigan JD, Chock S. Prospective assessment of post traumatic amnesia: A comparison of the GOAT and the OGMS. J Head Trauma Rehabil 1990;5:65-72.
Nakagawa TA, Ashwal S, Mathur M, et al. Guidelines for the determination of brain death in infants and children: an update of the 1987 Task Force recommendations. Crit Care Med 2011;39: 2139–55.
Napolitani M et al. Transcranial magnetic stimulation combined with high-density EEG in altered states of consciousness. Brain Injury 2014;28(9):1180–9.
Narkase-Thompson R, Sherer M, Yablon A, Nick TG, Trzepacz. Acute confusion following traumatic brain injury. Brain Injury 2004:18(2):131-42.
Nakase-Richardson R, Whyte J, Giacino J, et al. Longitudinal outcome of patients with disordered consciousness in the NIDRR TBI Model Systems Programs. J Neurotrauma 2011;28:1–8.
Nakase-Richardson R, Whyte J, Giacino JT, et al. Longitudinal outcome of patients with disordered consciousness in the NIDRR TBI Model Systems programs. J Neurotrauma 2012;29(1):59–65.
Norup A, Siert L, Lykke Mortensen E. Emotional distress and quality of life in relatives with traumatic brain injury: The first month after injury. Brain Injury 2010;24(2), 81Y88.
Owen AM, Coleman MR, Boly M, Davis MH, Laureys S, Pickard JD. Detecting awareness in the vegetative state. Science 2006;313(5792):1402.
Owen AM, Schiff ND, Laureys S. A new era of coma and consciousness science. Prog. Brain Res 2009;177:399–411.
Pistoia F, Sacco S, Carolei A, Sara M. Corticomotor facilitation in vegetative state: results of a pilot study. Arch Phys Med Rehabil 2013;94:1599–1606.
Plum F, Posner J. The Diagnosis of Stupor and Coma, 3rd edn. F. A. Davis, 1982.
Poulsen I et al. Patients with the most severe traumatic brain injury benefit from rehabilitation. Brain Injury 2014;28(5-6):321.
Practice parameters: assessment and management of patients in the persistent vegetative state (summary statement). The Quality Standards Subcommittee of the American Academy of Neurology. Neurology 1995;45:1015–8.
Psykiatrisk ordbog. (red.) Bertelsen A et al. København: Hans Reitzels Forlag, 2000.
Rader MA, Alston J & Ellis DW. Sensory stimulation of severely brain-injured patients. Brain Inj 1989;3:141–7.
Raichle ME et al. A default mode of brain function. PNAS 2001;98(29:676-82.
Rosenthal M, Griffith ER, Kreutzer JS, Pentlan B, eds. Rehabilitation of the adult and child with traumatic brain injury. 3. udg. Philadelphia: FA Davis Company, 1999.
Russel WR. Cerebral involvement in head injury: a study based on the examination of two hundred cases. Brain 1932;55:549-603.
Russel WR, Nathan PW. Traumatic Amnesia. Brain 1946;69:280-300.
Russel WR et al. Post-Traumatic Amnesia in Closed Head Injury. Arch Neurol 1961;5(1):4-17.
Sara M, Pistoia F, Mura E, Onorati P, Govoni S. Intrathecal baclofen in patients with persistent vegetative state: 2 hypotheses. Arch Phys Med Rehabil 2009;90:1245–9.
Schiff ND et al. Words without mind. J Cogn Neurosci 1999;11(6):650–6.
Schiff, ND et al. fMRI reveals large-scale network activation in minimally conscious patients. Neurology 2005;64(3): 514–5 23.
Schiff ND. Multimodal Neuroimaging Approaches to Disorders of Consciousness. J Head Trauma Rehabil 2006;21(5):388-97.
Schiff ND et al. Behavioural improvements with thalamic stimulation after severe traumatic brain injury. Nature 2007;448:600–3.
Schiff ND. Recovery of consciousness after brain injury: a mesocircuit hypothesis. Trends Neurosci 2010;33:1–9.
Schnakers O et al. Pain assessment and management in disorders of consciousness. Curr Opin Neurol 2007;20:620-6.
Schnakers C et al. Diagnostic accuracy of the vegetative and minimally conscious state: clinical consensus versus standardized neurobehavioral assessment. BMC Neurol 2009;9:35.
Schnakers O et al. Ethical implications: pain, coma, and related disorders. Encyclopedia of Consciousness 2009;1:243-50.
Schulman GL et al. Top-down Modulation of Early Sensory Cortex. Cerebral Cortex 1997;7:193–206.
Seel RT, Sherer M et al. American Congress of Rehabilitation Medicine, Brain Injury-Interdisciplinary Special Interest Group, Disorders of Consciousness Task Force, Assessment scales for disorders of consciousness: evidence-based recommendations for clinical practice and research. Arch Phys Med Rehabil 2010;91(12):1795–1813.
Seel RT et al. Specialized early treatment for persons with disorders of consciousness: program components and outcomes. Arch Phys Med Rehab 2013;94(10):1908-23.
Seeley WW et al. Dissociable intrinsic connectivity networks for salience processing and executive control. J Neurosci 2007;27(9):2349-56.
Sherer M et al. Multidimensional assessment of acute confusion after traumatic brain injury. Arch Phys Med rehabil 2005;86(5):896-904.
Sherer M, Yablon SA, Nakase-Richardson R, Nick TG. Effect of severity of post-traumatic confusion and its constituent symptoms on outcome after traumatic brain injury. Arch Phys Med Rehabil 2008;89:42–7.
Sherer M, Yablon SA, Nakase-Richardson R. Patterns of recovery of posttraumatic confusional state in neurorehabilitation admissions after traumatic brain injury. Arch Phys Med Rehabil 2009;90(10):1749–54.
Shiel A et al. The Wessex Head Injury Matrix (WHIM) main scale: a preliminary report on a scale to assess and monitor patient recovery after severe head injury. Clin Rehabil 2000;14:408–16.
Shores EA et al. Comparison of the Westmead PTA Scale and Glasgow Coma Scale as predictors of neuro-psychological outcome following extremely severe blunt head injury. J Neurol Neurosurg Psychiatry 1989;52:126-7.
Sidaros A, Herning M. Magnetisk resonans-skanning ved svær traumatisk hjerneskade. Ugeskr Læger 2007;169(3):214-6.
Sidaros A et al. Long-term global and regional brain volume changes following severe traumatic brain injury: A longitudinal study with clinical coerrelates. Neuroimage 2009;44:1-8.
Silver BV, Yablon SA. Akathisia resulting from traumatic brain injury. Brain Injury 1996;10:609-14.
Singh R et al. Zolpidem in a minimally conscious state. Brain Injury 2008;22:103–6.
Shridharan D et al. A critical role for the right fronto-insular cortex in switching between central-executive and default-mode networks. PNAS 2007;105(34):12569-74.
Soddu A et al. Identifying the dfault-mode component in spatial IC analysis of patients with disorders of consciousness. Hum Brain Mapp 2012;33:778-96.
Spector A et al. Efficacy of an evidence-based cognitive stimulation therapy programme for people with dementia: Randomised controlled trial. British J of Psychiatry 2003;183:248-54.
Stedaman JH, Graham JG. Head Injuries: an analysis and follow-up study. Proceedings of the Royal Society og Medicine 1970;63:23-8.
Stender J et al. The Minimal Energetic Requirement of Sustained Awareness after Brain Injury. Curr Biol 2016;26(11):1494:9.
Stone JL, Hughes JR. Early history of electroencephalography and establishment of the American Clinical Neurophysiology Society. J Clin Neurophysiol 2013;30(1):28-44.
Stuss DT, Binns MA, Carruth FG et al. The acute period of recovery from traumatic brain injury: Post traumatic amnesia or post traumatic confusional state? J Neurosurg 1999;90:635-43.
Symmonds CP, Russel WR. Accidental head injuries. Lancet 1943;1:7-10.
Taira T. Intrathecal administration of GABA agonists in the vegetative state. Prog Brain Res 2009;177:317–28.
Tate RL et al. A multicenter, randomized trial examining the effect of test procedures measuring emergence from post-traumatic amnesia. Journal of Neurology, Neurosurgery and Psychiatry 2006;77(7):841-9.
Teasdale G, Jennett B. Assessment of coma and impaired consciousness - a practical scale. Lancet 1974;2:81-4.
The Quality Standards Subcommittee of the American Academy of Neurology. Practice parameters: assessment and management of patients in the persistent vegetative state (summary statement). Neurology 1995;45(5):1015–18.
Thonnard M et al. Effect of zolpidem in chronic disorders of consciousness: a prospective open-label study. Funct. Neurol 2013;28(4):259–64.
Vanhaudenhuyse A et al. Default network connectivity reflects the level of consciousness in non-communicative brain-damaged patients. Brain 2010;133:161-71.
Van der Naalt J, van Zomeren AH et al. Acute behavioural disturbances related to imaging studies and outcome mild-to-moderate head injury. Brain Injury 2000;14:781-8.
Vogt BA, Laureys S. Posterior cingulate, precuneal and retrosplenial cortices: cytology and components of the neural network. Progress in brain research 2005;150:205–17.
Voss HU et al. Possible axonal regrowth in late recovery from the minimally conscious state. J Clin Invest 2006; 116:2005–11.
Whyte J, DiPasquale MC, Vaccaro M. Assessment of command-following in minimally conscious brain injured patients. Arch Phys Med Rehabil 1999;80:653–60.
Whyte J. Training and retention of rehabilitation researchers. Am J Phys Med Rehabil 2005;84(12):969-75.
Whyte J. Treatments to enhance recovery from the vegetative and minimally conscious states: ethical issues surrounding efficacy studies. Am J Phys Med Rehabil 2007;86:86–92.
Whyte J, Myers R. Incidence of clinically significant responses to zolpidem among patients with disorders of consciousness: a preliminary placebo controlled trial. Am J Phys Med Rehabil 2009;88:410–18.
Whyte J et al. Medical complications during inpatient rehabilitation among patients with traumatic disorders of consciousness. Arch Phys Med Rehabil 2013;94:1877–83.
Wijdicks EF et al. Validation of a New Coma Scale: The FOUR Score. Ann Neurol 2005;58:585–93.
Wilson BA, Evans JJ et al. Measuring recovery from post traumatic amnesia. Brain Injury 1999;13:5-20
--Christina Engelmann 8. feb 2017, 14:18 (UTC)